题目内容
【题目】水的离子积常数KW与温度t(℃)的关系如图所示: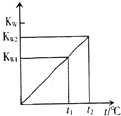
(1)若t1=25℃,则KW1=;若t2=100℃时,KW2=10﹣12 , 则0.05molL﹣1的Ba(OH)2溶液的pH= .
(2)已知25℃时,0.1L0.1molL﹣1的NaA溶液的pH=10,则NaA溶液中所存在的化学平衡有(用离子方程式表示): . 溶液中各离子的物质的量浓度由大到小的顺序为 .
(3)25℃时,将pH=11的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液pH=9,则NaOH溶液与硫酸溶液的体积比为 .
(4)100℃时,若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH(pH酸)与强碱的pH(pH碱)之间应满足的关系为:pH(酸)+pH(碱)= .
【答案】
(1)10﹣14;11
(2)A﹣+H2O?HA+OH﹣ , H2O?H++OH﹣;c(Na+)>c(A﹣)>c(OH﹣)>c(H+)
(3)1:9
(4)13
【解析】解:(1)在25℃,则Kw=10﹣14 , 根据pH=﹣lgc(H+)=﹣lg ![]() =11,所以答案是:10﹣14;11;(2)由于0.1L 0.1mo/L的NaA溶液的pH=10,说明溶液显示碱性,属于强碱弱酸盐,存在平衡A﹣+H2OHA+OH﹣ , H2OH++OH﹣ , 故不水解的钠离子浓度大于A﹣离子浓度,溶液显碱性,氢离子浓度大于氢氧根离子浓度,所以答案是:A﹣+H2OHA+OH﹣ , H2OH++OH﹣;c(Na+)>c(A﹣)>c(OH﹣)>c(H+);(3)设氢氧化钠溶液的体积为xL,硫酸溶液的体积为yL,pH=11的NaOH溶液中,氢氧根离子的浓度为:10﹣3mol/L,pH=4的硫酸溶液中氢离子浓度为:10﹣4mol/L,二者混合后溶液的pH=9,溶液酸性碱性,溶液中氢氧根离子的浓度为10﹣5mol/L,即氢氧化钠过量,即10﹣3mol/L×xL﹣10﹣4mol/L×y=10﹣5mol/L(x+y),解得x:y=1:9,所以答案是:1:9;(4)设强酸溶液的pH为a,体积为10V,溶液中氢离子浓度为:10﹣amol/L;碱溶液的pH为b,体积为V,溶液中氢氧根离子的浓度为:10﹣(12﹣b)mol/L,混合后溶液呈中性,则满足溶液中氢离子的物质的量大于氢氧根离子的物质的量,即10﹣amol/L×10VL=10﹣(12﹣b)mol/L×VL,解得:1﹣a=b﹣12,a+b=13,所以答案是:13.
=11,所以答案是:10﹣14;11;(2)由于0.1L 0.1mo/L的NaA溶液的pH=10,说明溶液显示碱性,属于强碱弱酸盐,存在平衡A﹣+H2OHA+OH﹣ , H2OH++OH﹣ , 故不水解的钠离子浓度大于A﹣离子浓度,溶液显碱性,氢离子浓度大于氢氧根离子浓度,所以答案是:A﹣+H2OHA+OH﹣ , H2OH++OH﹣;c(Na+)>c(A﹣)>c(OH﹣)>c(H+);(3)设氢氧化钠溶液的体积为xL,硫酸溶液的体积为yL,pH=11的NaOH溶液中,氢氧根离子的浓度为:10﹣3mol/L,pH=4的硫酸溶液中氢离子浓度为:10﹣4mol/L,二者混合后溶液的pH=9,溶液酸性碱性,溶液中氢氧根离子的浓度为10﹣5mol/L,即氢氧化钠过量,即10﹣3mol/L×xL﹣10﹣4mol/L×y=10﹣5mol/L(x+y),解得x:y=1:9,所以答案是:1:9;(4)设强酸溶液的pH为a,体积为10V,溶液中氢离子浓度为:10﹣amol/L;碱溶液的pH为b,体积为V,溶液中氢氧根离子的浓度为:10﹣(12﹣b)mol/L,混合后溶液呈中性,则满足溶液中氢离子的物质的量大于氢氧根离子的物质的量,即10﹣amol/L×10VL=10﹣(12﹣b)mol/L×VL,解得:1﹣a=b﹣12,a+b=13,所以答案是:13.