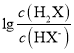题目内容
【题目】A、B、C、X为中学化学常见物质,A、B、C含有相同元素甲,一定条件下可以发生如下转化(水参与的反应,水未标出)。
![]()
(1)符合上述转化关系的A、X、B、C为____________________(填字母代号)
a.NaOHCO2Na2CO3NaHCO3 b.NaO2Na2ONa2O2
c.NH3 O2 NO NO2 d.FeCl2 FeCl2 FeCl3
(2)X为无色无味能使澄清石灰水变浑浊的气体,则C为_________________(填化学式)。若B中混有少量C杂质,除杂的化学方程式为_________________。
(3)C为红棕色气体,则A是_______或________(填化学式),若A的水溶液显碱性,写出A→B的化学方程式______________________________,B和C可相互转化,写出C→B的化学方程式_____________________________。
(4)若C为淡黄色固体,则B为___________,写出C在潜水艇中作为供氧剂牵涉的两个反应方程式__________、________。
(5)除(1)涉及的转化外,再写出一组符合转换关系的A、X、B、C ____ (填化学式)。
【答案】abc NaHCO3 2NaHCO3![]() Na2CO3+H2O+CO2↑ NH3 N2 4NH3+O2
Na2CO3+H2O+CO2↑ NH3 N2 4NH3+O2 4NO+4H2O 3NO2+H2O=2HNO3+NO Na2O 2Na2O2+2CO2=2Na2CO3+O2 2Na2O2+2H2O=4NaOH+O2↑ S(H2S)、O2、SO2、SO3
4NO+4H2O 3NO2+H2O=2HNO3+NO Na2O 2Na2O2+2CO2=2Na2CO3+O2 2Na2O2+2H2O=4NaOH+O2↑ S(H2S)、O2、SO2、SO3
【解析】
氢氧化钠溶液能与二氧化碳反应生成碳酸钠和水,二氧化碳能与碳酸钠溶液反应生成碳酸氢钠,符合上述转化关系;
常温下,钠与氧气反应生成氧化钠,加热条件下,氧化钠与氧气反应能生成过氧化钠,符合上述转化关系;
氨气在催化剂作用下,与氧气加热反应生成一氧化氮和水(或氮气在放电条件下,与氧气反应生成一氧化氮),一氧化氮与氧气反应生成二氧化氮,符合上述转化关系;
硫在氧气中燃烧生成二氧化硫(或硫化氢在氧气中燃烧生成二氧化硫和水),二氧化硫在催化剂作用下,二氧化硫与氧气共热反应生成三氧化硫。
(1)a.氢氧化钠溶液能与二氧化碳反应生成碳酸钠和水,二氧化碳能与碳酸钠溶液反应生成碳酸氢钠,符合上述转化关系,故正确;
b.常温下,钠与氧气反应生成氧化钠,加热条件下,氧化钠与氧气反应能生成过氧化钠,符合上述转化关系,故正确;
c.氨气在催化剂作用下,与氧气加热反应生成一氧化氮和水,一氧化氮与氧气反应生成二氧化氮,符合上述转化关系,故正确;
d.铁在氯气中燃烧只能生成氯化铁,不能生成氯化亚铁,不符合上述转化关系,故错误;
abc正确,故答案为:abc;
(2)若X为无色无味能使澄清石灰水变浑浊的气体,则X为二氧化碳、A为氢氧化钠、B为碳酸钠、C为碳酸氢钠;若碳酸钠中混有碳酸氢钠,可以用加热的方法除去碳酸氢钠,碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,反应的化学方程式为2NaHCO3![]() Na2CO3+H2O+CO2↑,故答案为:NaHCO3;2NaHCO3
Na2CO3+H2O+CO2↑,故答案为:NaHCO3;2NaHCO3![]() Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
(3)若C为红棕色气体,则X为氧气、A为氨气或氮气、B为一氧化氮、C为二氧化氮,若A的水溶液显碱性,A为氨气,氨气在催化剂作用下,与氧气加热反应生成一氧化氮和水,反应的化学方程式为4NH3+O2 4NO+4H2O;二氧化氮与水反应生成硝酸和一氧化氮,反应的化学方程式为3NO2+H2O=2HNO3+NO,故答案为:NH3;N2;4NH3+O2
4NO+4H2O;二氧化氮与水反应生成硝酸和一氧化氮,反应的化学方程式为3NO2+H2O=2HNO3+NO,故答案为:NH3;N2;4NH3+O2 4NO+4H2O;3NO2+H2O=2HNO3+NO;
4NO+4H2O;3NO2+H2O=2HNO3+NO;
(4)若C为淡黄色固体,则X为氧气、A为钠、B为氧化钠、C为过氧化钠,在潜水艇中,过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,与水反应生成氢氧化钠和氧气,反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑,故答案为:2Na2O2+2CO2=2Na2CO3+O2;2Na2O2+2H2O=4NaOH+O2↑;
(5)除(1)涉及的转化外,还可能存在与硫元素有关的物质间的转化,转化关系为硫在氧气中燃烧生成二氧化硫(或硫化氢在氧气中燃烧生成二氧化硫和水),二氧化硫在催化剂作用下,二氧化硫与氧气共热反应生成三氧化硫,则A为硫或硫化氢、X为氧气、B为二氧化硫、C为三氧化硫,故答案为:S(H2S)、O2、SO2、SO3。

 快乐5加2金卷系列答案
快乐5加2金卷系列答案【题目】研究铜和铁与浓硫酸的反应,实验如下:
① | ② |
| |
铜丝表面无明显现象 铁丝表面迅速变黑,之后无明显现象 | 铜丝或铁丝逐渐溶解,产生大量气体, 品红溶液褪色 |
下列说法正确的是
A. 常温下不能用铁制容器盛放浓硫酸,可用铜制容器盛放浓硫酸
B. ②中铜丝或铁丝均有剩余时,产生气体的物质的量相等
C. 依据②,可推断出铜和铁与浓硫酸反应可生成SO2
D. ①②中现象的差异仅是由于温度改变了化学反应速率
【题目】水体砷污染已成为一个亟待解决的全球性环境问题,我国科学家研究零价铁活化过硫酸钠(Na2S2O8)去除废水中的正五价砷[As(Ⅴ)],其机制模型如下。
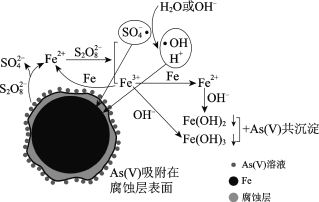
零价铁活化过硫酸钠去除废水中As(Ⅴ)的机制模型
资料:
Ⅰ.酸性条件下SO4·为主要的自由基,中性及弱碱性条件下SO4·和·OH同时存在,强碱性条件下·OH为主要的自由基。
Ⅱ.Fe2+、Fe3+形成氢氧化物沉淀的pH
离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe2+ | 7.04 | 9.08 |
Fe3+ | 1.87 | 3.27 |
(1)砷与磷在元素周期表中位于同一主族,其原子比磷多一个电子层。
① 砷在元素周期表中的位置是______。
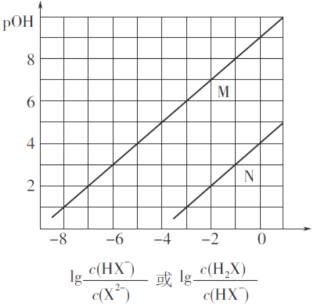
② 砷酸的化学式是______,其酸性比H3PO4______(填“强”或“弱”)。
(2)零价铁与过硫酸钠反应,可持续释放Fe2+,Fe2+与S2O82反应生成Fe3+和自由基,自由基具有强氧化性,利于形成Fe2+和Fe3+,以确保As(Ⅴ)去除完全。
①S2O82中S的化合价是______。
②零价铁与过硫酸钠反应的离子方程式是______。
③Fe3+转化为Fe2+的离子方程式是______。
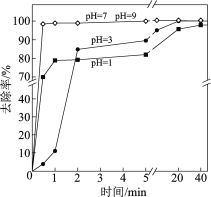
(3)不同pH对As(Ⅴ)去除率的影响如图。5 min内pH = 7和pH = 9时去除率高的原因是______。