题目内容
【题目】以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:

回答下列问题:
(1)在一定条件下,SO2转化为SO3的反应为2SO2+O2![]() 2SO3,该反应的平衡常数表达式为K=____;过量的SO2与NaOH溶液反应的化学方程式为_________________。
2SO3,该反应的平衡常数表达式为K=____;过量的SO2与NaOH溶液反应的化学方程式为_________________。
(2)用36.5%(密度为1.2g·㎝-3)的盐酸的配制500mL的30%(密度为1.095g·㎝-3的盐酸,所需玻璃仪器是 (___)
A.玻璃棒 B.烧杯 C.托盘天平 D.500mL量筒 E、500mL容量瓶 F、胶头滴管
(3)酸溶及后续过程中均需保持盐酸过量,其目的是________________________、
________________________________________________________。
(4)通氯气氧化时,发生的主要反应的离子方程式为_________________________;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为________________(写化学式)。
(5)操作a为_________________________、过滤、洗涤、干燥。
【答案】K=c2(SO3)/c(O2)·c2(SO2) SO2+NaOH=NaHSO3 ABDEF 提高铁元素的浸出率 抑制Fe3+水解 Cl2+2Fe2+=2Cl-+2Fe3+ Cl2、HCl 蒸发浓缩、冷却结晶
【解析】
根据流程可知,硫铁矿在高温下焙烧可以得到铁的氧化物,将其溶于盐酸中,可以得到含有亚铁离子、铁离子的盐溶液,向其中通入氯气,能将亚铁离子氧化为铁离子,最后得到的氯化铁溶液蒸发浓缩、冷却结晶后得到氯化铁晶体,据此分析作答。
(1)根据平衡常数的定义易知,该反应的化学平衡常数K=c2(SO3)/c(O2)·c2(SO2);过量的二氧化硫与氢氧化钠反应会生成亚硫酸氢钠,其化学方程式为:SO2+NaOH=NaHSO3;
(2)根据溶液配制的步骤分析可知,计算:结合c=![]() 可知,该浓盐酸的物质的量浓度为
可知,该浓盐酸的物质的量浓度为![]() mol/L=12mol/L,稀盐酸的物质的量浓度为
mol/L=12mol/L,稀盐酸的物质的量浓度为![]() =10.95mol/L,依据C浓V浓 = C稀V稀求出所需盐酸溶液的体积V浓=
=10.95mol/L,依据C浓V浓 = C稀V稀求出所需盐酸溶液的体积V浓=![]() =0.456L=456mL;量取:依据计算的体积,用500mL量筒量取;洗涤时需要用到烧杯和玻璃棒;移液时需要移到500mL容量瓶中,定容时需要胶头滴管,故所需的玻璃仪器有:A.玻璃棒、B.烧杯、D.500mL量筒、E. 500mL容量瓶、F. 胶头滴管,故答案为ABDEF;
=0.456L=456mL;量取:依据计算的体积,用500mL量筒量取;洗涤时需要用到烧杯和玻璃棒;移液时需要移到500mL容量瓶中,定容时需要胶头滴管,故所需的玻璃仪器有:A.玻璃棒、B.烧杯、D.500mL量筒、E. 500mL容量瓶、F. 胶头滴管,故答案为ABDEF;
(3)过量的盐酸可抑制铁离子的水解,提高铁离子的浸出率,故酸溶及后续过程中均需保持盐酸过量,其目的是提高铁元素的浸出率、抑制Fe3+水解;
(4)氯气与Fe2+反应生成Fe3+与Cl-,其离子方程式为:Cl2+2Fe2+=2Cl-+2Fe3+;该过程中尾气有过量的氯化氢与氯气,需用氢氧化钠吸收,故答案为Cl2、HCl;
(5)得到的氯化铁溶液蒸发浓缩、冷却结晶后得到氯化铁晶体,故答案为蒸发浓缩、冷却结晶。

【题目】下图所示的实验,能达到实验目的的是
A | B | C | D |
|
|
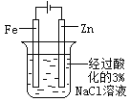
片刻后在 Fe 电极附近滴入铁氰化钾溶液 |
|
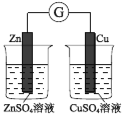
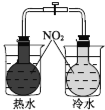
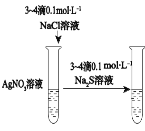
验证化学能转化为电能 | 证明温度对平衡移动的影响 | 验证 Fe 电极被保护 | 验证AgCl 溶解度大于Ag2S |
A.AB.BC.CD.D