ΧβΡΩΡΎ»ί
ΓΨΧβΡΩΓΩΘ®1Θ©OΜυΧ§‘≠Ή”ΚΥΆβΒγΉ”≈≈≤Φ ΫΈΣ____ΓΘH2O VSEPRΡΘ–ΆΟϊ≥ΤΈΣ_____Θ§ΝΔΧεΙΙ–ΆΈΣ___ΓΘO3____ΦΪ–‘Ζ÷Ή”Θ®ΧνΓΑ «Γ±ΜρΓΑ≤Μ «Γ±Θ©ΓΘ
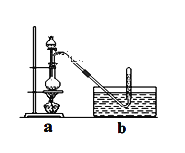
Θ®2Θ©άϊ”Ο»»Μ·―ßΖ®ά¥≤βΕ®ΨßΗώΡή «”…Born”κHaber Ήœ»Χα≥ωά¥ΒΡΘ§Τδ Β÷ «άϊ”ΟHessΕ®¬…Θ§ΙΙ≥…“ΜΗω»»Μ·―ß―≠ΜΖΓΘ
“―÷ΣΘΚNa(s)+ ![]() Cl2(g)= NaCl(s) ΠΛH=Θ≠410.9 kJΓΛmolΘ≠1
Cl2(g)= NaCl(s) ΠΛH=Θ≠410.9 kJΓΛmolΘ≠1
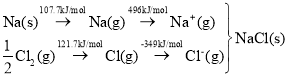
Ω…÷ΣΘ§Na‘≠Ή”ΒΡΒΎ“ΜΒγάκΡήΈΣ_____kJΓΛmolΘ≠1ΘΜCl-ClΦϋΦϋΡήΈΣ______kJΓΛmolΘ≠1ΘΜNaClΨßΗώΡήΈΣ_____kJΓΛmolΘ≠1ΓΘ
Θ®3Θ©ΗΏ―Ιœ¬NaCl ΨßΧεΚΆ Na Μρ Cl2 Ζ¥”ΠΘ§Ω…“‘–Έ≥…≤ΜΆ§Ήι≥…ΓΔ≤ΜΆ§ΫαΙΙΒΡΨßΧεΘ§»γΆΦ «Τδ÷–“Μ÷÷ΨßΧεΒΡΨßΑϊΘ®¥σ«ρΈΣ¬»‘≠Ή”Θ§ –Γ«ρΈΣΡΤ‘≠Ή”Θ©Θ§ΤδΜ·―ß ΫΈΣ________ΓΘ
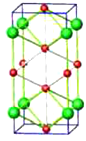
Θ®4Θ©Ϋπ τNaΨßΧε÷–ΒΡ‘≠Ή”Ε―ΜΐΖΫ Ϋ≥ΤΈΣΧε–ΡΝΔΖΫΕ―ΜΐΘ§ΨßΑϊ≤Έ ΐΈΣa nmΘ§Ω’Φδάϊ”Ο¬ ΈΣ________Θ®Ν–≥ωΦΤΥψ ΫΘ©ΓΘ
ΓΨ¥πΑΗΓΩ1s22s22p4 ΥΡΟφΧε–Έ V–Έ « 496 243.4 787.3 Na2Cl 
ΓΨΫβΈωΓΩ
(1)ΗυΨίΚΥΆβΒγΉ” ΐ≈≈≤ΦΘ§Φέ≤ψΒγΉ”ΜΞ≥βάμ¬έΚΆ‘”Μ·ΙλΒάάμ¬έΖ÷ΈωΫβ¥πΘΜάϊ”ΟΒ»ΒγΉ”ΧεΒΡΫαΙΙΧΊΒψΖ÷ΈωΫβ¥πΘΜ
(2)ΤχΧ§ΜυΧ§Na‘≠Ή” ß»Ξ1ΗωΒγΉ”ΉΣΜ·ΈΣΤχΧ§ΜυΧ§ΡΤάκΉ”–η“ΣΒΡΉνΒΆΡήΝΩΈΣNaΒΡΒΎ“ΜΒγάκΡήΘΜCl-ClΦϋΒΡΦϋΡήΒ»”Ύ1molCl2–Έ≥… Cl(g)ΥυΈϋ ’ΒΡΡήΝΩΘΜNaClΨßΗώΡή «Na+ΓΔCl-ΤχΧ§άκΉ”–Έ≥…1molNaClΨßΧε ΆΖ≈ΒΡΡήΝΩΘΜ
(3)ΗυΨί“ΜΗωΨßΑϊ÷–Ης‘≠Ή”Ζ÷±π‘ΎάβΓΔ±ΏΓΔΟφΒΡΥυ‘Ύ±»άΐΦΤΥψΜ·―ß ΫΘΜ
(4)Ω’Φδάϊ”Ο¬ =ΨßΑϊ÷–‘≠Ή”Υυ’ΦΉήΧεΜΐ”κΨßΑϊΧεΜΐΒΡ±»÷ΒΓΘ
(1) O‘≠Ή”ΈΣ8Κ≈‘ΣΥΊΘ§ΚΥΆβΒγΉ” ΐ≈≈≤Φ ΫΈΣΘΚ1s22s22p4Θ§H2O÷–÷––Ρ―θ‘≠Ή”≥…ΦϋΒγΉ”Ε‘ ΐΈΣ2Θ§Ι¬ΒγΉ”Ε‘ ΐ «2Θ§ΦέΒγΉ”Ε‘ ΐ «4Θ§‘ρVSEPRΡΘ–ΆΟϊ≥ΤΈΣΥΡΟφΧεΘ§ΝΔΧεΙΙ–ΆΈΣV–Έ ΘΜO3ΚΆSO2 «Β»ΒγΉ”ΧεΘ§SO2÷–ΈΣV–ΆΖ÷Ή”Θ§’ΐΓΔΗΚΒγΚ…÷––Ρ≤Μ÷ΊΚœΘ§ «ΦΪ–‘Ζ÷Ή”Θ§Β»ΒγΉ”ΧεΒΡΫαΙΙœύΥΤΘ§O3 «ΦΪ–‘Ζ÷Ή”ΘΜ
(2)ΤχΧ§ΜυΧ§Na‘≠Ή” ß»Ξ1ΗωΒγΉ”ΉΣΜ·ΈΣΤχΧ§ΜυΧ§ΡΤάκΉ”–η“ΣΒΡΉνΒΆΡήΝΩΈΣNaΒΡΒΎ“ΜΒγάκΡήΘ§Ι NaΒΡΒΎ“ΜΒγάκΡήΈΣ496kJ/molΘΜClCΦϋΒΡΦϋΡήΡήΒ»”Ύ1molCl2–Έ≥…Cl(g)ΥυΈϋ ’ΒΡΡήΝΩΘ§Ι ClClΦϋΡή=2ΓΝ121.7kJ/mol=243.4kJ/molΘΜNaClΨßΗώΡή «Na+ΓΔClΤχΧ§άκΉ”–Έ≥…1molNaClΨßΧε ΆΖ≈ΒΡΡήΝΩΘ§ΗυΨίΠΛH=EΈϋ-EΖ≈Θ§Ι NaClΒΡΨßΗώΡή= EΈϋ-ΠΛH=(496+107+121.7-349) kJ/mol ®C(Θ≠410.9 kJΓΛmolΘ≠1)=787.3kJ/molΘΜ
(3)ΨßΑϊ÷–4ΗωNa‘≠Ή”‘Ύάβ…œΘ§2ΗωNa‘≠Ή”‘ΎΟφ–ΡΘ§2ΗωNa‘≠Ή”‘ΎΨßΑϊΡΎ≤ΩΘ§‘ρΡΤ‘≠Ή” ΐΝΩ=4ΓΝ![]() +2ΓΝ
+2ΓΝ![]() +2=4Θ§8ΗωCl‘≠Ή”‘Ύάβ…œΘ§‘ρ¬»‘≠Ή”ΒΡ ΐΝΩ=8ΓΝ
+2=4Θ§8ΗωCl‘≠Ή”‘Ύάβ…œΘ§‘ρ¬»‘≠Ή”ΒΡ ΐΝΩ=8ΓΝ![]() =2Θ§‘ρΗΟΨßΧεΒΡΜ·―ß ΫΈΣNa2ClΘΜ
=2Θ§‘ρΗΟΨßΧεΒΡΜ·―ß ΫΈΣNa2ClΘΜ
(4)Ϋπ τNaΨßΧε÷–ΒΡ‘≠Ή”Ε―ΜΐΖΫ Ϋ≥ΤΈΣΧε–ΡΝΔΖΫΕ―ΜΐΘ§ΤδΕ―ΜΐΖΫ Ϋ»γΆΦΥυ ΨΘΚ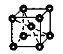 Θ§‘ρ“ΜΗωΨßΑϊ÷–ΡΤ‘≠Ή” ΐΝΩ=8ΓΝ
Θ§‘ρ“ΜΗωΨßΑϊ÷–ΡΤ‘≠Ή” ΐΝΩ=8ΓΝ![]() +1=2Θ§ΨßΑϊ≤Έ ΐΈΣa nmΘ§‘ρΨßΑϊΒΡΧεΜΐΈΣV(ΨßΑϊ)= a3nm3Θ§ΗυΨίΨßΑϊΆΦ ΨΘ§ΨßΑϊΧεΕ‘Ϋ«œΏΒΡ≥ΛΕ»=4r(Na)Θ§‘ρr(Na)=
+1=2Θ§ΨßΑϊ≤Έ ΐΈΣa nmΘ§‘ρΨßΑϊΒΡΧεΜΐΈΣV(ΨßΑϊ)= a3nm3Θ§ΗυΨίΨßΑϊΆΦ ΨΘ§ΨßΑϊΧεΕ‘Ϋ«œΏΒΡ≥ΛΕ»=4r(Na)Θ§‘ρr(Na)=![]() nmΘ§‘ρΨßΑϊ÷–ΡΤ‘≠Ή”ΒΡΉήΧεΜΐ=2ΓΝ
nmΘ§‘ρΨßΑϊ÷–ΡΤ‘≠Ή”ΒΡΉήΧεΜΐ=2ΓΝ![]() Θ§‘ρΨßΑϊΩ’Φδάϊ”Ο¬ =
Θ§‘ρΨßΑϊΩ’Φδάϊ”Ο¬ = ΓΘ
ΓΘ

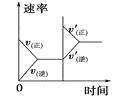
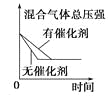
ΓΨΧβΡΩΓΩΕ‘”ΎΩ…ΡφΖ¥”ΠN2(g)+3H2(g) ![]() 2NH3(g) ΓςH<0Θ§œ¬Ν–―–ΨΩΡΩΒΡΚΆ Ψ“βΆΦœύΖϊΒΡ «Θ® Θ©
2NH3(g) ΓςH<0Θ§œ¬Ν–―–ΨΩΡΩΒΡΚΆ Ψ“βΆΦœύΖϊΒΡ «Θ® Θ©
A | B | C | D | |
―–ΨΩΡΩΒΡ | ―Ι«ΩΕ‘Ζ¥”ΠΒΡ”Αœλ Θ®p2ΘΨp1Θ© | Έ¬Ε»Ε‘Ζ¥”ΠΒΡ”Αœλ | ΤΫΚβΧεœΒ÷–‘ωΦ”N2ΒΡ≈®Ε»Ε‘Ζ¥”ΠΒΡ”Αœλ | ¥ΏΜ·ΦΝΕ‘Ζ¥”ΠΒΡ”Αœλ |
Ψ“βΆΦ |
|
|
|
|
A.AB.BC.CD.D
ΓΨΧβΡΩΓΩ(1)Μ·―ßΖ¥”ΠΩ… ”ΈΣΨ…ΦϋΕœΝ―ΚΆ–¬Φϋ–Έ≥…ΒΡΙΐ≥ΧΓΘΜ·―ßΦϋΒΡΦϋΡή «–Έ≥…(Μρ≤πΩΣ)1molΜ·―ßΦϋ ± ΆΖ≈(ΜρΈϋ ’)≥ωΒΡΡήΝΩΓΘ“―÷ΣΑΉΝΉ(P4)ΚΆP4O6ΒΡΖ÷Ή”ΫαΙΙ»γΆΦΥυ ΨΘ§

“―÷ΣΘΚ
Μ·―ßΦϋ | PΓΣP | PΓΣO | O=O |
ΦϋΡή(kJΓΛmol1) | 198 | 360 | 498 |
‘ρΖ¥”ΠP4(g)+3O2(g)= P4O6(g)ΒΡΓςH=_________ΓΘ
(2)“―÷ΣΔΌ2C(s)+O2(g)=2CO(g) ΓςH=-221.0kJ/mol
ΔΎ2H2(g)+O2(g)=2H2O(g) ΓςH=-483.6kJ/mol
‘ρ÷Τ±ΗΥ°ΟΚΤχΒΡΖ¥”ΠC(s)+H2O(g)=CO(g)+ H2(g)ΒΡΓςH=_______ΓΘ