题目内容
2.某含碳、氢、氧三种元素的有机物,其C、H、O的质量比为6:1:8,它的实验式为CH2O;该有机物蒸气的密度是相同条件下氢气密度的30倍,则该有机物的分子式为C2H4O2.分析 设他们的质量分别是6x,x,8x,则C的物质的量为$\frac{6x}{12}$=$\frac{x}{2}$; H的物质的量为 $\frac{x}{1}$=x;O的物质的量为 $\frac{8x}{16}$=$\frac{x}{2}$,所以物质的量之比为1:2:1,所以实验式为CH2O,又因为该有机物蒸气的密度是相同条件下氢气密度的30倍,则它的相对分子量为2×30=60,而一个CH2O的分子量为30,从而就出有机物的分子式,由此解答.
解答 解:设碳、氢、氧三种元素的质量分别是6x,x,8x,则C的物质的量为$\frac{6x}{12}$=$\frac{x}{2}$; H的物质的量为 $\frac{x}{1}$=x;O的物质的量为 $\frac{8x}{16}$=$\frac{x}{2}$,所以物质的量之比为1:2:1,所以实验式为CH2O,又因为该有机物蒸气的密度是相同条件下氢气密度的30倍,则它的相对分子量为2×30=60,而一个CH2O的分子量为30,所以有机物的分子式C2H4O2,
故答案为:CH2O;C2H4O2.
点评 本题考查了有机物分子式与结构的确定,难度不大,所以根据三种元素的质量之比来确定分子的实验式,最后确定分子式.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
12.有八种物质:①甲烷、②苯、③聚乙烯、④丙烯 ⑤2-丁炔、⑥环己烷、⑦环己烯,既能使酸性高锰酸钾溶液褪色,又能使溴水因反应而褪色的是( )
| A. | ③④⑤ | B. | ④⑤⑦ | C. | ④⑤ | D. | ③④⑤⑦⑧ |
13.工业上,为使95.6%的乙醇变为100%的绝对乙醇,常常加入一种物质加热回流一段时间后蒸馏,得到99.5%的无水乙醇,这种物质是( )
| A. | 无水硫酸 | B. | 无水氯化钙 | C. | 生石灰 | D. | 浓硫酸 |
10.有一多肽其化学式为C55H70O19N10,将其彻底水解后只得到下列四种氨基酸:
甘氨酸(H2N-CH2COOH),丙氨酸(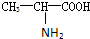 ),苯丙氨酸(
),苯丙氨酸(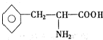 )
)
谷氨酸(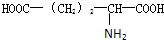 ),则该多肽中所含肽键的数目以及水解后得到的谷氨酸和苯丙氨酸的数目分别是( )
),则该多肽中所含肽键的数目以及水解后得到的谷氨酸和苯丙氨酸的数目分别是( )
甘氨酸(H2N-CH2COOH),丙氨酸(
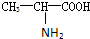 ),苯丙氨酸(
),苯丙氨酸( )
)谷氨酸(
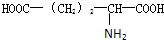 ),则该多肽中所含肽键的数目以及水解后得到的谷氨酸和苯丙氨酸的数目分别是( )
),则该多肽中所含肽键的数目以及水解后得到的谷氨酸和苯丙氨酸的数目分别是( )| A. | 10,4,3 | B. | 10,3,4 | C. | 9,4,3 | D. | 9,3,4 |
14.R的气态氢化物为RH3,则R元素最高价氧化物的水化物的化学式可能是( )
| A. | H3RO4 | B. | H2RO4 | C. | HRO4 | D. | H2RO3 |
11.相同物质的量的下列各烃,完全燃烧后消耗氧气最多的是( )
| A. | 甲烷 | B. | 乙烷 | C. | 乙烯 | D. | 乙炔 |
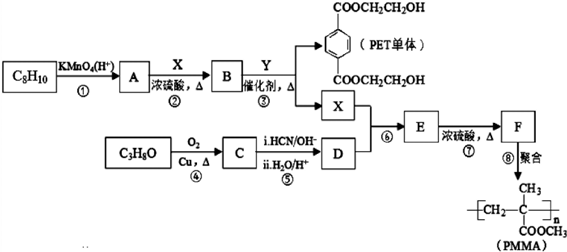
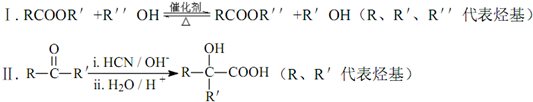
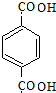 .
.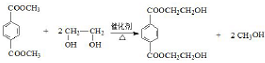 .
.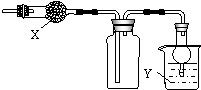 如图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是( )
如图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是( ) ;A元素形成的气态氢化物中A原子的杂化类型为sp3;
;A元素形成的气态氢化物中A原子的杂化类型为sp3;