题目内容
【题目】设![]() 为阿伏加德罗常数的值,某二元酸(简写为
为阿伏加德罗常数的值,某二元酸(简写为![]() )溶液按下式电离:
)溶液按下式电离:![]() ,
,![]() ,关于常温下的下列溶液叙述错误的是( )
,关于常温下的下列溶液叙述错误的是( )
A.![]()
![]() 的
的![]() 溶液的
溶液的![]() 数目为
数目为![]()
B.在![]() 质量分数为46%的
质量分数为46%的![]() 水溶液中,含氧原子总数为
水溶液中,含氧原子总数为![]()
C.![]()
![]() 的
的![]() 溶液中
溶液中![]() 、
、![]() 、
、![]() 、
、![]() 总的粒子数为
总的粒子数为![]()
D.![]() 溶液中一定存在
溶液中一定存在![]()
【答案】C
【解析】
A.常温下pH=2的H2A溶液,则溶液中氢离子浓度是0.01mol/L,因此1L溶液中H+数目为0.01 NA,A正确;
B.100g质量分数为46%的H2A水溶液中,H2A的质量为46克,水的质量为54g,即物质的量为3mol,氧原子总数为3NA,B正确;
C.由电离方程式可以知道H2A的一级电离为完全电离,二级电离为部分电离,所以HA-不发生水解,溶液中不存在H2A,C错误;
D.Na2A溶液中A2-存在水解,溶液存在Na+、H+、HA-、A2-、OH-,电荷守恒有c(Na+)+c(H+)=c(HA-)+2c(A2-)+c(OH-),D正确。
故选C。

【题目】二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。二氧化硫有毒,并且是形成酸雨的主要气体。无论是实验室制备还是工业生产,二氧化硫尾气吸收或烟气脱硫都非常重要。
完成下列填空:
(1)实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫。
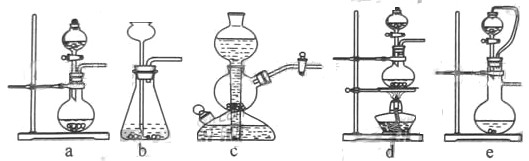
如果用硫酸和亚硫酸钠反应制取二氧化硫,并希望能控制反应速度,上图中可选用的发生装置
是________(填写字母)。
(2)若用硫酸和亚硫酸钠反应制取3,36L(标准状况)二氧化硫,至少需要称取亚硫酸钠______g(保留一位小数);如果已有4.0%亚硫酸钠(质量分数),被氧化成硫酸钠,则至少需称取该亚硫酸钠______g (保留一位小数)。
(3)实验室二氧化硫尾气吸收与工业烟气脱硫的化学原理相通。石灰-石膏法和碱法是常用的烟气脱硫法。
石灰-石膏法的吸收反应为SO2+Ca(OH)2→CaSO3↓+H2O。吸收产物亚硫酸钙由管道输送至氧化塔氧化,反应为2CaSO3+O2+4H2O→2CaSO4·2H2O。其流程如下图:
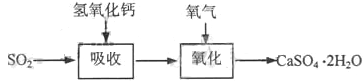
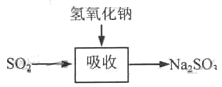
碱法的吸收反应为SO2+2NaOH→Na2SO3+H2O。碱法的特点是氢氧化钠碱性强、吸收快、效率高。其流程如下图:
已知:
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.9 |
吸收SO2的成本(元/mol) | 0.027 | 0.232 |
石灰-石膏法和碱法吸收二氧化硫的化学原理相同之处是____________________。和碱法相比,石灰-石膏法的优点是________________,缺点是________________。
(4)在石灰-石膏法和碱法的基础上,设计一个改进的、能实现物料循环的烟气脱硫方案(用流程图表示)________________。