题目内容
工业上用固体硫酸亚铁制取颜料铁红(Fe2O3),反应原理是:2FeSO4![]() Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑
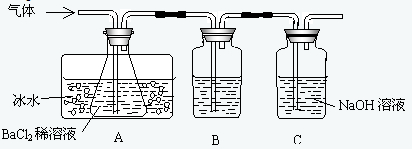
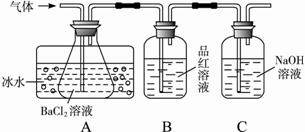
某研究性学习小组用下图所示装置分别检验该反应所产生的气态物质,然后利用装置A瓶内的生成物来测定已分解的FeSO4的质量。(已知:SO2沸点为-10.02 ℃)

请完成相关问题:
(1)本实验中,A瓶所盛BaCl2溶液可以吸收的气体是____________,发生反应的离子方程式为__________________。
(2)B瓶所盛的试剂的作用是__________________________________;C瓶所盛试剂的作用是____________________________________________。
(3)A瓶要用冷水冷却的原因是______________________________________。
(4)某学生欲利用装置B反应前后的质量差确定已分解的FeSO4质量,你认为该同学方案是否合理________(填“合理”“不合理”),理由是________________________________。
(5)依据上述装置和反应事实,请设计测定已分解的FeSO4质量的操作和方法:________
________________________________。
(1)SO3 SO3+H2O+Ba2+====BaSO4↓+2H+
(2)检验生成的SO2 吸收未完全反应的SO2,防止污染空气
(3)因为SO3溶解放热,防止形成酸雾,使SO3吸收完全
(4)不合理(1分) 品红溶液不能将SO2完全吸收
(5)将装置A中的沉淀过滤、洗涤、干燥、称量,依据称量结果(BaSO4的质量)计算出已分解硫酸亚铁质量。(如果用称量A装置的质量变化来确定已分解硫酸亚铁质量酌情给分)
解析:(1)因为SO2与BaCl2不反应。

工业上用固体硫酸亚铁制取颜料铁红(Fe2O3)反应原理是:2FeSO4Fe2O3+SO2↑+SO3↑,某学生欲检验该反应所产生的气态物质,依次将气体通过盛有(Ⅰ)BaCl2溶液、(Ⅱ)X溶液、(Ⅲ)NaOH溶液的三个装置。则下列对该方案的评价中正确的是( )
| A.(Ⅰ)中会生成BaSO3、BaSO4两种沉淀 |
| B.可将(Ⅰ)中的BaCl2溶液改为Ba(NO3)2溶液 |
| C.(Ⅱ)所盛X可为品红溶液 |
| D.(Ⅲ)的作用是吸收有毒的SO2气体 |