题目内容
下列说法中错误的是
| A.化学反应中的能量变化通常表现为热量的变化 |
| B.化学键的断裂和形成是化学反应中能量变化的主要原因 |
| C.反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量 |
| D.需要加热才能发生的化学反应一定是吸热反应 |
D
解析试题分析:A.化学反应的过程是旧键断裂、新键形成的过程,所以通常伴随着能量变化。而这种能量变化通常表现为热量的变化。正确。B.化学反应的过程就是原子重新组合的过程。在这个过程中,反应物中的化学键断裂消耗能量。原子形成化学键又释放能量。化学键的断裂和形成是化学反应中能量变化的主要原因。正确。C.如果反应物总能量高于生成物总能量的总能量,发生的反应就是放热反应,否则就是吸热反应。所以二者的相对大小决定了反应是放出能量还是吸收能量。正确。D.任何反应的发生都需要一个活化的过程。这与反应是否是放热或吸热反应无关。错误。
考点:考查化学反应过程中的能量变化的知识。

酸碱中和反应 NaOH(?)+ HCl(?)→NaCl(?)+ H2O(?)+57.6 kJ中,问号表示的状态正确的是
| A.NaOH:固 | B.盐酸:液 | C.NaCl:溶液 | D.H2O:溶液 |
(6分)(2012?重庆)肼(H2N﹣NH2)是一种高能燃料,有关化学反应的能量变化如图所示,已知断裂1mol化学键所需的能量(kJ):N≡N为942、O=O为500、N﹣N为154,则断裂1molN﹣H键所需的能量(kJ)是( )
| A.194 | B.391 | C.516 | D.658 |
氯原子对O3的分解有催化作用:O3+Cl=ClO+O2 ΔH1,ClO+O=Cl+O2 ΔH2。大气臭氧层的分解反应是:O3+O=2O2 ΔH,该反应的能量变化如图所示,则下列叙述正确的是( )。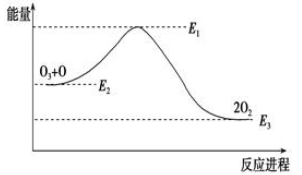
①反应O3+O=2O2的ΔH=E1-E3 ②反应O3+O=2O2是放热反应 ③ΔH=ΔH1+ΔH2 ④大气层中的臭氧无法再生
| A.①② | B.②③ | C.③④ | D.②④ |
有关键能数据如下表所示: 
则晶体硅在氧气中燃烧的热化学方程式为 ;
;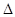 H="-989.2"
H="-989.2" 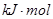
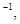 则x的值为 ( )
则x的值为 ( )
| A.460 | B.920 | C.1 165.2 | D.423.3 |
下列图示与对应的叙述相符的是 
| A.图Ⅰ中 可以看出反应A(g)=C(g)的△H=(E1-E4)kJ·mol-1 |
B.图Ⅱ表示一定条件下进行的反应2SO2+O2 2SO3 各成分的物质的量变化,t2时刻改变的条件可能是扩大了容器的体积 2SO3 各成分的物质的量变化,t2时刻改变的条件可能是扩大了容器的体积 |
| C.图Ⅲ表示将CO2通入NaOH的稀溶液中,随着CO2的通入,溶液中水电离出的c(H+)变化关系 |
| D.图Ⅳ曲线表示用0.1000mol/LNaOH溶液分别滴定浓度相同的三种一元酸,由此可判断HX的酸性最强 |
SF6是一种优良的绝缘气体,分子结构中只存在S-F键。已知:1molS(s)转化为气态硫原子吸收能量280kJ,断裂1molF-F 、S-F键需吸收的能量分别为160kJ、330kJ。则S(s)+3F2(g)=SF6(g)的反应热△H为
| A.-1780kJ/mol | B.-1220 kJ/mol | C.-450 kJ/mol | D.+430 kJ/mol |
某一化学反应在不同条件下的能量变化曲线如右图所示。下列说法正确的是
| A.化学催化比酶催化的效果好 |
| B.使用不同催化剂可以改变反应的热效应 |
| C.使用不同催化剂可以改变反应的能耗 |
| D.反应物的总能量低于生成物的总能量 |