��Ŀ����
��ԭ�Ӷ�O3�ķֽ��д����ã�O3��Cl��ClO��O2����H1��ClO��O��Cl��O2����H2������������ķֽⷴӦ�ǣ�O3��O��2O2����H���÷�Ӧ�������仯��ͼ��ʾ��������������ȷ����(����)��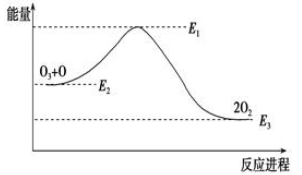
�ٷ�ӦO3��O��2O2�Ħ�H��E1��E3���ڷ�ӦO3��O��2O2�Ƿ��ȷ�Ӧ���ۦ�H����H1����H2���ܴ������еij���������
| A���٢� | B���ڢ� | C���ۢ� | D���ڢ� |
B
���������������ͼ��֪��������������ͣ�O+O3=2O2 �ķ�ӦΪ���ȷ�Ӧ����H=E3-E2���ʢٴ���O+O3=2O2 �ķ�ӦΪ���ȷ�Ӧ����H=E3-E2���ʢ���ȷ����Cl+O3=ClO+O2 ��H1��ClO+O=Cl+O2 ��H2��֪�����ݸ�˹����������Ӧ��ӵõ�O+O3=2O2 ������H=��H1+��H2���ʢ���ȷ�������зŵ�ʱ������ת��Ϊ��������������еij��������������ʢܴ���ѡB��
���㣺���黯ѧ��Ӧ�е������仯����˹����

��������������������������������Ľ��죬�о���ѧ��Ӧ���������仯�Ժ������ó�����Դ�Ϳ�������Դ����ʮ����Ҫ�����塣����˵���в���ȷ����
| A���κλ�ѧ��Ӧ�������������ı仯 |
| B����ѧ��Ӧ�е������仯������Ϊ�����ı仯 |
| C����Ӧ������������������������������Ӧ�ͷ����� |
| D������ѧ���γ�ʱ�ͷŵ�����С�ھɻ�ѧ�����ƻ�ʱ��Ҫ���յ���������Ӧ�������� |
��ҡҡ������һ�ּ��ü�������ϡ���ʳʱ�����Ϲ�����еĻ�ѧ���ʺ�ˮ��Ϻ�ҡ���������䡣�û�ѧ������ �� ��
| A���Ȼ��� | B����������� | C�������������� | D����ʯ�� |
��ѧ��Ӧһ���������������仯����H2��O2��ȼ�յķ�Ӧ����ȷ���ǡ�
| A���÷�ӦΪ���ȷ�Ӧ������������ | B���÷�ӦΪ���ȷ�Ӧ�� �� |
| C������H��H���ų��������� | D������H��O���������� |
���й����Ȼ�ѧ��Ӧ����������ȷ���� (����)
| A����֪H��(aq)��OH��(aq)��H2O(l)����H����57.3 kJ��mol��1����H2SO4��Ba(OH)2��Ӧ�ķ�Ӧ�Ȧ�H��2��(��57.3) kJ��mol��1 |
B��ȼ�ϵ���н��״�����ת��Ϊ�������Ȼ�ѧ����ʽ��CH3OH(g)��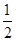 O2(g)===CO2(g)��2H2(g)��H����192.9 kJ��mol��1����CH3OH(g)��ȼ����Ϊ192.9 kJ��mol��1 O2(g)===CO2(g)��2H2(g)��H����192.9 kJ��mol��1����CH3OH(g)��ȼ����Ϊ192.9 kJ��mol��1 |
| C��H2(g)��ȼ������285.8 kJ��mol��1����2H2O(g)===2H2(g)��O2(g)����H��571.6 kJ��mol��1 |
D�������ǵ�ȼ������2 800 kJ��mol��1����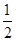 C6H12O6(s)��3O2(g)===3CO2(g)��3H2O(l)����H����1 400 kJ��mol��1 C6H12O6(s)��3O2(g)===3CO2(g)��3H2O(l)����H����1 400 kJ��mol��1 |
����˵���д������
| A����ѧ��Ӧ�е������仯ͨ������Ϊ�����ı仯 |
| B����ѧ���Ķ��Ѻ��γ��ǻ�ѧ��Ӧ�������仯����Ҫԭ�� |
| C����Ӧ��������������������������Դ�С�����˷�Ӧ�Ƿų����������������� |
| D����Ҫ���Ȳ��ܷ����Ļ�ѧ��Ӧһ�������ȷ�Ӧ |
ij��Ӧ�ķ�Ӧ�����������仯��ͼ��ʾ(ͼ��E1��ʾ����Ӧ�Ļ�ܣ�E2��ʾ�淴Ӧ�Ļ��)�������й�������ȷ����( ) 
| A���÷�ӦΪ���ȷ�Ӧ |
| B���÷�Ӧ�ʱ�ɱ�ʾΪ��H������E1��E2��kJ��mol-1 |
| C�������ܽ��ͷ�Ӧ�Ļ�� |
| D�������ܸı䷴Ӧ���ʱ� |
��(N2H4)�ֳ���������һ�ֿ�ȼ�Ե�Һ�壬���������ȼ�ϡ���֪��
N2(g)+2O2(g)��2NO2(g) ��H=+67.7kJ/mol,
2N2H4(g)+2NO2(g)��3N2(g)+4H2O(g) ��H=��1135.7kJ/mol��
����˵����ȷ����
| A��N2H4(g)+O2(g)��N2(g)+2H2O(g) ��H=��1068 kJ/mol |
| B�������백���Ƶ������������ˮ������뷽��ʽ��N2H4 + H2O��N2H5��+ OH�� |
| C�������缫����KOH��ҺΪ�������Һ���¡�����ȼ�ϵ�أ��ŵ�ʱ�ĸ�����Ӧʽ��N2H4��4e��+4OH����N2��+4H2O |
| D�������缫����KOH��ҺΪ�������Һ���¡�����ȼ�ϵ�أ�����һ��ʱ���KOH��Һ��pH������ |


 N2O4(g)�У������ʵ�Ũ��������������֮��Ĺ�ϵ�����н���A��Ӧ��״̬Ϊ��ѧƽ��״̬
N2O4(g)�У������ʵ�Ũ��������������֮��Ĺ�ϵ�����н���A��Ӧ��״̬Ϊ��ѧƽ��״̬ ������t2
������t2