��Ŀ����
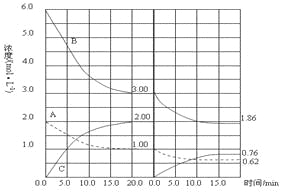
����Ŀ��ijͬѧ�������ݻ���ͬ���ܱ������У��ֱ��о����ֲ�ͬ�����»�ѧ��Ӧ2X(g)![]() Y(g)��W(g)�Ľ������������ʵ��������������T1��ʵ����������T2�����ǵ���ʼŨ�Ⱦ���c(X)��1.0 mol��L��1��c(Y)��c(W)��0����÷�Ӧ��X��Ũ����ʱ��ı仯��ͼ��ʾ������˵������ȷ����(����)
Y(g)��W(g)�Ľ������������ʵ��������������T1��ʵ����������T2�����ǵ���ʼŨ�Ⱦ���c(X)��1.0 mol��L��1��c(Y)��c(W)��0����÷�Ӧ��X��Ũ����ʱ��ı仯��ͼ��ʾ������˵������ȷ����(����)

A.��ʵ������ȣ�ʵ��������ʹ���˴���
B.��ʵ������ȣ�ʵ������ֻ�ı��¶ȣ����¶�T1<T2���÷�Ӧ�����ȷ�Ӧ
C.��ʵ�������������У��ﵽƽ��״̬ʱX������ٷֺ�����ͬ
D.����ʼŨ��c(X)��0.8 mol��L��1��c(Y)��c(W)��0������������ʵ������ͬ����ƽ��Ũ��c(X)��0.4 mol��L��1
���𰸡�C
��������
A����ͼ��֪��ʵ��������ƽ���ʱ��̣�ƽ��ʱʵ������ʵ������X��Ũ�Ȳ��䣬˵����Ӱ��ƽ���ƶ����÷�Ӧǰ����������ʵ������䣬�ʿ���Ϊ����ѹǿ��ʹ�ô�����ѡ��A��ȷ��
B���¶�Խ�߷�Ӧ����Խ�죬����ƽ���ʱ��Խ�̣����¶�T1��T2���¶�Խ�ߣ�ƽ��ʱX��Ũ��ԽС��˵�������¶�ƽ��������Ӧ�����ƶ���������Ӧ�����ȷ�Ӧ��ѡ��B��ȷ��
C����ͼ��֪��ʵ��I��II��ʱX��Ũ����ȣ�ʵ����ƽ��ʱX��Ũ��С��X�����ʵ���С���÷�Ӧǰ����������ʵ������䣬ʵ����ƽ��ʱX������ٷֺ�����ʵ��I��II�ͣ�ѡ��C����
D����ͼ��֪��ʵ��������ƽ��ʱX��Ũ��Ϊ0��5mol/L����X��Ũ�ȱ仯��Ϊ1mol/L-0��5mol/L��0��5mol/L��Xת����Ϊ![]() ��50%����ʼŨ��c��X����0��8mol/L��Ũ�Ƚ��ͣ�ѹǿ��С���÷�Ӧǰ����������ʵ������䣬ƽ�ⲻ�ƶ���X��ת���ʲ��䣬��ƽ��Ũ��c��X����0��8mol/L��50%��0��4mol/L��ѡ��D��ȷ��
��50%����ʼŨ��c��X����0��8mol/L��Ũ�Ƚ��ͣ�ѹǿ��С���÷�Ӧǰ����������ʵ������䣬ƽ�ⲻ�ƶ���X��ת���ʲ��䣬��ƽ��Ũ��c��X����0��8mol/L��50%��0��4mol/L��ѡ��D��ȷ��
��ѡC��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ����֪�������ݣ�
���� | �۵�/�� | �е�/�� | �ܶ�/g��cm��3 |
�Ҵ� | ��144 | 78.0 | 0.789 |
���� | 16.6 | 118 | 1.05 |
�������� | ��83.6 | 77.5 | 0.900 |
Ũ����(98%) | �� | 338 | 1.84 |
��ͼΪʵ������ȡ����������װ��ͼ��

��1��������̼������Һ�Ϸ��ռ����϶�Һ��ʱ��ֹͣ���ȣ�ȡ��С�Թ�B����������á���ǰ���ʵ������Ϊ________(����ĸ)��
A���ϲ�Һ��䱡 B���²�Һ���ɫ��dz���Ϊ��ɫ C����������� D���й���ζ
��2��Ϊ���������������Ҵ�������Ļ����ɰ����в�����з��룺

���Լ�1���ѡ��_________________________________________________��
�ڲ���1��________�����õ���Ҫ����������__________________________��
���Լ�2���ѡ��_____________________________________��
�ܲ���2��_______________________________________��
�ݲ���3���¶ȼ�ˮ�����λ��ӦΪ��ͼ��________(�a����b����c����d��)��ʾ���ڸò����У���������ƿ���¶ȼ��� ����ƿ ������Ҫ�IJ���������__________��________��________���ռ�����������¶���________��

����Ŀ����ҵ�����õ�ⱥ��ʳ��ˮ����ȡ�ռ���õ�ʳ��ˮ�����ξ��ơ���һ�ξ�����Ҫ���ó�������ȥ����ˮ��Ca2+��Mg2+��Fe3+��SO42-�����ӣ��������£�
��.�����ˮ�м������BaCl2��Һ�����ˣ�
��.��������Һ�м������Na2CO3��Һ�����ˣ�
��.�����������Һ��pH�����һ�ξ�����ˮ��
(1)���̢��г�ȥ��������______��
(2)���ǹ��̢������ɵIJ��ֳ���������20��ʱ���ܽ��(g/100 gH2O)��
CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 | Fe(OH)3 |
2.6��10-2 | 2.5��10-4 | 7.8��10-4 | 2.4��10-4 | 1.7��10-3 | 4.8��10-9 |
���ñ�����Ϣ�ش��������⣺
�ٹ��̢������ɵ���Ҫ������CaCO3��Mg2(OH)2CO3���______��
�ڹ��̢�ѡ�õ���BaCl2����ѡ��CaCl2��ԭ����______��
�۳�ȥMg2+�����ӷ���ʽ��______��
�ܼ��Ca2+��Mg2+��Ba2+�Ƿ����ʱ��ֻ����Ba2+���ɣ�ԭ����______��
(3)�ڶ��ξ���Ҫ��ȥ����I-��IO3-��NH4+��Ca2+��Mg2+������ʾ��ͼ��ͼ��
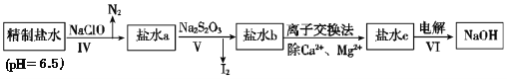
�ٹ��̢���ȥ��������______��
����ˮb�к���SO42-��Na2S2O3��IO3-��ԭΪI2�����ӷ���ʽ��______��
���ڹ��̢������õ�Na2S2O3�׳ƺ�������һ����Ҫ�Ļ���ԭ�ϡ���Ʒ������Ҫ�ɷ���Na2S2O3��5H2OΪ�˲ⶨ�京Na2S2O3��5H2O�Ĵ��ȣ���ȡ8.00 g��Ʒ�����Ƴ�250.0 mL��Һ��ȡ25.00 mL����ƿ�У��μӵ�����Һ��ָʾ��������Ũ��Ϊ0.0500 mol/L�ĵ�ˮ�ζ�(������Ӧ2S2O32-+I2=S4O62-+2I-)���ζ��ﵽ�յ�ʱ��������______���±���¼�ζ������
�ζ����� | �ζ�ǰ����(mL) | �ζ��ζ������(mL) |
��һ�� | 0.30 | 31.12 |
�ڶ��� | 0.36 | 31.56 |
������ | 1.10 | 31.88 |
������Ʒ�Ĵ���Ϊ______��