题目内容
7.二氧化硫能使溴水褪色,说明二氧化硫具有( )| A. | 还原性 | B. | 氧化性 | C. | 漂白性 | D. | 酸性 |
分析 二氧化硫与溴水发生氧化还原反应生成氢溴酸和硫酸.
解答 解:二氧化硫具有还原性,与溴水发生氧化还原反应生成氢溴酸和硫酸,使溴水褪色,硫元素化合价升高,体现还原性.
故选A.
点评 本题主要考查了二氧化硫的性质,侧重考查二氧化硫的还原性,注意中间价态的元素既有氧化性又有还原性,同种元素相邻价态间不发生氧化还原反应,题目难度不大.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
18.配置240mL1.84mol•L-1稀硫酸,下列操作正确的是( )
| A. | 将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却 | |
| B. | 必须的定量仪器有100mL量筒、250mL容量瓶和托盘天平 | |
| C. | 量取质量分数为98%的浓硫酸(ρ=1.84g•cm-3)的体积为25.0mL | |
| D. | 先在容量瓶中加入适量水,将量好的浓硫酸注入容器瓶加入定容 |
15.某元素原子核内含有23个质子,则该元素基态原子内未成对的电子数为( )
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 5个 |
2.有机物经核磁共振检测,给出3种信号的有( )
| A. | CH3OH | B. | CH3CH2CH3 | ||
| C. | 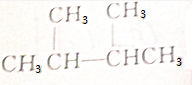 | D. | CH3COOCH2CH3 |
12.下列有关物质性质的比较,错误的是( )
| A. | 溶解度:小苏打<苏打 | B. | 密度:溴乙烷>水 | ||
| C. | 硬度:晶体硅<金刚石 | D. | 碳碳键键长:乙烯>苯 |
19.工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2.在该反应中( )
| A. | 硫元素既被氧化又被还原 | |
| B. | 氧化剂与还原剂的物质的量之比为1:2 | |
| C. | 每生成1molNa2S2O3,转移4mol电子 | |
| D. | 相同条件下,每吸收10m3SO2就会放出2.5m3CO2 |
16. 已知电解熔融氧化钙可以得到金属钙和氯气,钙在氯气中燃烧又能生成氯化钙.请你根据已学知识,按图中箭头所表示的物质间可能发生的转化,分析下列说法正确的是( )
已知电解熔融氧化钙可以得到金属钙和氯气,钙在氯气中燃烧又能生成氯化钙.请你根据已学知识,按图中箭头所表示的物质间可能发生的转化,分析下列说法正确的是( )
 已知电解熔融氧化钙可以得到金属钙和氯气,钙在氯气中燃烧又能生成氯化钙.请你根据已学知识,按图中箭头所表示的物质间可能发生的转化,分析下列说法正确的是( )
已知电解熔融氧化钙可以得到金属钙和氯气,钙在氯气中燃烧又能生成氯化钙.请你根据已学知识,按图中箭头所表示的物质间可能发生的转化,分析下列说法正确的是( )| A. | CaO、Ca(OH)2、CaCO3三者都是离子化合物,在固态时可以导电 | |
| B. | 工业上也可用电解熔融氧化钙的方法制备金属钙 | |
| C. | 往Ca(OH)2溶液中滴加Na2CO3溶液或NaHCO3溶液,都能实现⑥的转化 | |
| D. | 工业上以氯气和石灰乳为原料通过反应制造主要成分为CaCl2的漂白粉 |
 L B.
L B. L C.
L C. L D.
L D. L
L