题目内容
12.下列有关物质性质的比较,错误的是( )| A. | 溶解度:小苏打<苏打 | B. | 密度:溴乙烷>水 | ||
| C. | 硬度:晶体硅<金刚石 | D. | 碳碳键键长:乙烯>苯 |
分析 A.相同条件下,碳酸钠溶解度大于碳酸氢钠;
B.卤代烃的密度比水大;
C.原子晶体中,键长越短,键能越大,则硬度越大;
D.苯中碳碳键介于单键和双键之间.
解答 解:A.在碳酸钠饱和溶液中通入二氧化碳生成碳酸氢钠,可观察到溶液变浑浊,说明碳酸钠溶解度大于碳酸氢钠,故A正确;
B.卤代烃的密度比水大,则溴乙烷的密度大于水,故B正确;
C.晶体硅与金刚石都为原子晶体C-C<Si-Si,原子晶体中,键长越短,键能越大,则硬度越大,故C正确;
D.苯中碳碳键介于单键和双键之间,碳碳键键长:乙烯<苯,故D错误.
故选D.
点评 本题考查元素及其对应单质、化合物的性质的递变规律,侧重于溶解度、硬度、密度等性质的考查,题目难度不大,注意把握性质比较的角度以及规律.

练习册系列答案
 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
2.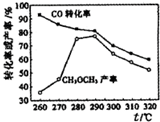 研究者在某条件下探究制备二甲醚反应:2CO(g)+4H2(g)?CH3 OCH3(g)+H2 O(g)△H,测定结果如图所示.下列判断错误的是( )
研究者在某条件下探究制备二甲醚反应:2CO(g)+4H2(g)?CH3 OCH3(g)+H2 O(g)△H,测定结果如图所示.下列判断错误的是( )
 研究者在某条件下探究制备二甲醚反应:2CO(g)+4H2(g)?CH3 OCH3(g)+H2 O(g)△H,测定结果如图所示.下列判断错误的是( )
研究者在某条件下探究制备二甲醚反应:2CO(g)+4H2(g)?CH3 OCH3(g)+H2 O(g)△H,测定结果如图所示.下列判断错误的是( )| A. | △H<0 | |
| B. | 该反应伴随有副反应的发生 | |
| C. | 制备二甲醚的适宜温度为280~290℃ | |
| D. | 加入催化剂可以提高CH3 OCH3的产率 |
3.在pH=9的NaOH溶液和CH3COONa溶液中,水电离的OH-浓度分别为M mol/L和N mol/L,M和N的关系为( )
| A. | M>N | B. | M=10-4N | C. | N=10-4M | D. | M=N |
7.二氧化硫能使溴水褪色,说明二氧化硫具有( )
| A. | 还原性 | B. | 氧化性 | C. | 漂白性 | D. | 酸性 |
17.下列反应中的氨与反应4NH3+5O2→4NO+6H2O中的氨作用相同的是( )
| A. | 2Na+2NH3→2NaNH2+H2↑ | B. | 2NH3+3CuO→3Cu+N2+3H2O | ||
| C. | 4NH3+6NO→5N2+6H2O | D. | 3SiH4+4NH3→Si3N4+12H2 |
19.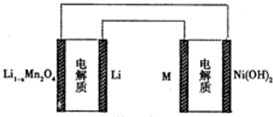 某充电宝锂离子电池的总反应为:xLi+Li1-nMn2O4$?_{充电}^{放电}$LiMn2O4,某手机镍氢电池总反应为:NiOOH+MH$?_{充电}^{放电}$M+Ni(OH)2(M为储氢金属或合金),有关上述 两种电池的说法不正确的是
某充电宝锂离子电池的总反应为:xLi+Li1-nMn2O4$?_{充电}^{放电}$LiMn2O4,某手机镍氢电池总反应为:NiOOH+MH$?_{充电}^{放电}$M+Ni(OH)2(M为储氢金属或合金),有关上述 两种电池的说法不正确的是
( )
 某充电宝锂离子电池的总反应为:xLi+Li1-nMn2O4$?_{充电}^{放电}$LiMn2O4,某手机镍氢电池总反应为:NiOOH+MH$?_{充电}^{放电}$M+Ni(OH)2(M为储氢金属或合金),有关上述 两种电池的说法不正确的是
某充电宝锂离子电池的总反应为:xLi+Li1-nMn2O4$?_{充电}^{放电}$LiMn2O4,某手机镍氢电池总反应为:NiOOH+MH$?_{充电}^{放电}$M+Ni(OH)2(M为储氢金属或合金),有关上述 两种电池的说法不正确的是( )
| A. | 锂离子电池放电时Li+向正极迁移 | |
| B. | 锂离子电池充电时,阴极的电极反应式:LiMn2O4-xe-=Li1-nMn2O4+xLi+ | |
| C. | 如图表示用锂离子电池给镍氢电池充电 | |
| D. | 镍氢电池放电时,正极的电极反应式:NiOOH+H2O+e-=Ni(OH)2+OH- |