题目内容
【题目】SiC、GaN、GaP、GaAs等是人工合成半导体的材料,具有高温、高频、大功率和抗辐射的应用性能而成为半导体领域研究热点。试回答下列问题:
(1)碳的基态原子L层电子轨道表达式为__,砷属于__区元素。
(2)N与氢元素可形成一种原子个数比为1:1的粒子,其式量为60,经测定该粒子中有一正四面体构型,判断该粒子中存在的化学键__。
A.配位键 B.极性共价键 C.非极性共价键 D.氢键
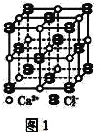
(3)CaC2晶体的晶胞结构与NaCl晶体的相似(如图1所示),但CaC2晶体中含有的哑铃形C22-的存在,使晶胞沿一个方向拉长。CaC2晶体中1个Ca2+周围距离最近的C22-数目为__。
【答案】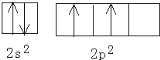 p ABC 4
p ABC 4
【解析】
![]() 碳原子的L层有4个电子,2个在2S上,2个在2P上,且自旋相同,碳的基态原子L层电子轨道表达式为
碳原子的L层有4个电子,2个在2S上,2个在2P上,且自旋相同,碳的基态原子L层电子轨道表达式为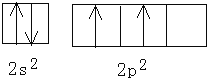 ,砷原子的外围电子排布为
,砷原子的外围电子排布为![]()
故答案为: ;p;
;p;
![]() 氮原子之间形成非极性键,氮原子和氢原子之间形成极性键,氢原子和氮原子之间形成配位键,
氮原子之间形成非极性键,氮原子和氢原子之间形成极性键,氢原子和氮原子之间形成配位键,
故答案为:ABC;
![]() 根据图知,以最中心钙离子为例,
根据图知,以最中心钙离子为例,![]() 晶体中1个
晶体中1个![]() 周围距离最近的
周围距离最近的![]() 数目为4,
数目为4,
故答案为:4。

 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案【题目】二氧化氮可由NO和O2生成,已知在2 L密闭容器内,800 ℃时反应:2NO(g)+O2(g) 2NO2(g) ΔH, n(NO)、n(O2)随时间的变化如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.200 | 0.100 | 0.080 | 0.050 | 0.050 | 0.050 |
n(O2)/mol | 0.100 | 0.050 | 0.040 | 0.025 | 0.025 | 0.025 |
(1)该反应的化学平衡常数表达式为K=___________________
(2)已知:K800 ℃>K1 000 ℃,则该反应的ΔH_________0(填“大于”或“小于”),
(3)用O2表示0~2 s内该反应的平均速率为_________。
(4)能说明该反应已达到平衡状态的是_________。
a.容器内气体颜色保持不变 b.2υ逆(NO)=υ正(O2)
c.容器内压强保持不变 d.容器内气体密度保持不变
(5)为使该反应的速率增大,提高NO的转化率,且平衡向正反应方向移动,应采取的措施有____。
A.升温 B.加入氧气 C. 降温 D.增大压强
(6)在800 ℃时,计算通入2 mol NO和1 mol O2的平衡常数K=_________
(7)已知下列反应在某温度下的平衡常数以及ΔH
H2(g)+S(s) H2S(g) K1 ΔH1
S(s)+O2(g) SO2(g) K2 ΔH2
则在该温度下反应H2(g)+SO2(g) O2(g)+H2S(g) K3 ΔH3
平衡常数K3=__________(用含有K1 K2的式子表示);
其反应热ΔH3=________(用含有ΔH1 ΔH2的式子表示)