题目内容
【题目】下列递变规律正确的是( )
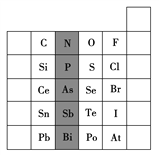
A. HClO4、H2SO4、H3PO4的酸性依次增强 B. 钠、镁、铝的还原性依次减弱
C. HCl、HBr、HI的稳定性依次增强 D. P、S、Cl原子半径逐渐增大
【答案】B
【解析】A. Cl、S、P的非金属性依次减弱,故HClO4、H2SO4、H3PO4的酸性依次减弱,A不正确;B. 钠、镁、铝的金属性依次减弱,故其单质的还原性依次减弱,B正确; C. Cl、Br、I的非金属性依次减弱,故HCl、HBr、HI的稳定性依次减弱,C不正确;D. P、S、Cl原子半径逐渐减小,D不正确。本题选B。

【题目】1 L某混合溶液,可能含有的离子如下表:
阳离子 | H+、K+、Mg2+、Al3+、NH4+、Fe2+、Fe3+ |
阴离子 | Cl-、Br-、I-、CO32-、AlO2- |
(1)向该溶液中逐滴加入cmol/L NaOH溶液,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示。则该溶液中一定含有的离子是______________。
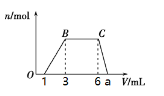
(2)根据图像数据计算a=_______________mL
(3)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1 L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:
Cl2的体积(标准状况) | 2.8 L | 5.6 L | 11.2 L |
n(Cl-) | 1.25 mol | 1.5 mol | 2 mol |
n(Br-) | 1.5 mol | 1.4 mol | 0.9 mol |
n(I-) | x mol(x≠0) | 0 | 0 |
①当通入Cl2的体积为5.6L时,溶液中发生反应的离子方程式为______________。
②原溶液中Cl-、Br-、I-的物质的量浓度之比为____________________________。
③x=_________________mol