��Ŀ����
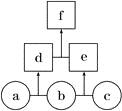
����Ŀ��Ԫ�������ڱ��е�λ�ã���ӳ��Ԫ�ص�ԭ�ӽṹ��Ԫ�ص����ʡ���ͼ��Ԫ�����ڱ���һ���֡�
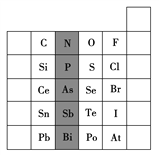
(1)��Ӱ����Ԫ��N��Ԫ�����ڱ��е�λ��Ϊ____���ڵ�____�塣����Ԫ�������ɣ�Ԥ������ǿ����H3AsO4____H3PO4(�>����<��)��
(2)S������ϼۺ���ͻ��ϼ۵Ĵ�����Ϊ____����һ�������£�S��H2��Ӧ��һ����(������Ϊ��Ӧ���еij̶�)�����жϣ�����ͬ������Se��H2��Ӧ�ij̶ȱ�S��H2��Ӧ�̶�____(�������С������ͬ��)��
(3)Br2���н�ǿ�������ԣ�SO2���н�ǿ�Ļ�ԭ�ԣ���SO2����ͨ����ˮ����Һ�д��ڵ���Ҫ������____��
(4)����˵���������____(�����)��
��C��N��O��F��ԭ�Ӱ뾶����ԭ���������������С
��Si��P��S��ClԪ�صķǽ��������ź˵���������Ӷ���ǿ
�۸ɱ�������Һ̬ˮת��Ϊ��̬ˮ��Ҫ�˷������ڵĹ��ۼ�
��HF��HCl��HBr��HI�����ȶ������μ���
���𰸡���1��2��VA��<����2��4����С����3��H����Br����SO42-��4��C
��������
������Ҫ����Ԫ�������ɡ�
(1)��Ӱ����Ԫ��N��Ԫ�����ڱ��е�λ��Ϊ���ڵ�VA�塣����Ԫ�������ɣ��ǽ�����ǿ����As<P����������ǿ����H3AsO4<H3PO4��
(2)S������ϼۺ���ͻ��ϼ۵Ĵ�����Ϊ4����һ�������£�S��H2��Ӧ��һ����(������Ϊ��Ӧ���еij̶�)���ǽ�����Sǿ��Se�����жϣ�����ͬ������Se��H2��Ӧ�ij̶ȱ�S��H2��Ӧ�̶ȸ�С��
(3)Br2���н�ǿ�������ԣ�SO2���н�ǿ�Ļ�ԭ�ԣ���SO2����ͨ����ˮ��Br2�߱���ԭΪBr-��SO2������ΪSO![]() ��ͬʱ����H+����Һ�д��ڵ���Ҫ������H����Br����SO
��ͬʱ����H+����Һ�д��ڵ���Ҫ������H����Br����SO![]() ��
��
(4)����˵��������Ǣۡ���C��N��O��FԪ������ͬ����Ԫ�أ�C��N��O��F��ԭ�Ӱ뾶����ԭ���������������С���ʢ���ȷ����Si��P��S��ClԪ������ͬ����Ԫ�أ�Si��P��S��ClԪ�صķǽ��������ź˵���������Ӷ���ǿ���ʢ���ȷ���۸ɱ�������Һ̬ˮת��Ϊ��̬ˮ��Ҫ�˷����Ӽ����������ʢ۴��ܷǽ����ԣ�F>Cl>Br>I������HF��HCl��HBr��HI�����ȶ������μ������ʢ���ȷ����ѡ�ۡ�

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�����Ŀ�����ҹ��涨������ˮ�����ŷŵ��������Ũ��Ϊ0.005 mg/L���������ӷ�ˮ�ɲ��û�ѧ���������Իش��������⣺
��1�������ӣ�Cd3(PO4)2�������ܽ�ƽ�ⳣ���ı���ʽKsp��________��
��2��һ���¶��£�CdCO3��Ksp��4.0 �� 10-12��Cd��OH��2��Ksp��3.2 �� 10-14����ô������ˮ�е��ܽ���________�ϴ�
��3����ij���ӷ�ˮ�м���Na2S����S2-Ũ�ȴﵽ7.9 �� 10-8mol/Lʱ��ˮ����Cd2+Ũ��Ϊ_____mol/L����֪��Ksp��CdS��=7.9 �� 10-27��Ar(Cd)=112������ʱ�Ƿ����ˮԴ����______����������������������
����п�̳�����Ҫ�ɷ�ΪZnO��������CuO��FeO��Ϊԭ�ϣ�������ȡ�Ȼ�п�ͽ���п����ȡ�Ȼ�п��Ҫ�������£�
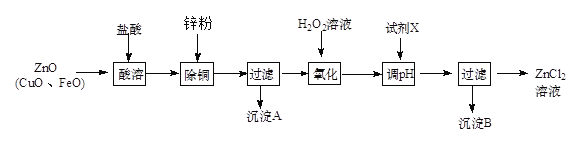
�±��г�����ؽ������������������������pH (��ʼ������pH����������Ũ��Ϊ1.0 mol��L��1����)��
�������� | Fe3+ | Zn2+ | Fe2+ |
��ʼ������pH | 1. 1 | 5. 2 | 5. 8 |
������ȫ��pH | 3. 2 | 6. 4 | 8. 8 |
��1������H2O2��Һ��������________________��
��2������ͼ�У�����pHʱ��������Լ�X������________������ţ�
A��ZnO B��NaOH C��Zn2(OH)2CO3 D��ZnSO4
pHӦ������_________��