题目内容
16.下列对氧化还原反应的分析正确的是( )| A. |  | B. |  | ||
| C. | 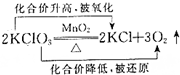 | D. |  |
分析 A.反应中H元素的化合价降低得电子;
B.Fe失电子被氧化;
C.反应中K的化合价不变;
D.反应中Fe的化合价降低,C的化合价升高.
解答 解:A.反应中H元素的化合价降低得电子,O元素的化合价升高,即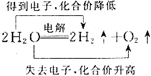 ,故A错误;
,故A错误;
B.Fe失电子被氧化,S得电子被还原,即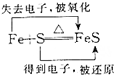 ,故B错误;
,故B错误;
C.反应中K的化合价不变,Cl元素的化合价降低被还原,O元素的化合价升高被氧化,即 ,故C错误;
,故C错误;
D.反应中Fe的化合价降低,被还原,C的化合价升高,被氧化,即 ,故D正确.
,故D正确.
故选D.
点评 本题考查氧化还原反应及电子转移,把握反应物与生成物及反应中元素的化合价判断为解答的关键,题目难度不大.

练习册系列答案
相关题目
6.实验是解决化学问题的基本途径,下列有关实验的叙述不正确的是( )
| A. | 240 mL 0.2 mol•L-1的NaOH溶液配制:需要使用天平、烧杯、250 mL容量瓶等仪器 | |
| B. | 除去Cu粉中的CuO,可向混合物中滴加适量稀硫酸再过滤 | |
| C. | 为增强氯水的漂白性,向其中加入碳酸钙 | |
| D. | 为使0.5mol/L的NaNO3溶液物质的量浓度变为1mol/L,可将原溶液加热蒸发掉50克水 |
7.如图是课外活动小组设计的用化学电源使LED灯发光的装置.下列说法错误的是( )
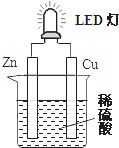

| A. | 铜片表面有气泡生成,且铜片为正极,为电子流入的一极 | |
| B. | 如果将硫酸换成苹果汁,导线中不会有电子流动 | |
| C. | 装置中存在“化学能→电能→光能”的转换 | |
| D. | 如果将锌片换成铁片,电路中的电流方向由铜片经导线流向铁片,铁片发生氧化反应 |
20.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1.0 L 1.0 mo1•L-1的NaAlO2 水溶液中含有的氧原子数为2 NA | |
| B. | 密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2 NA | |
| C. | 过氧化钠与水反应时,生成0.1 mol 氧气转移的电子数为0.2 NA | |
| D. | 标准状况下,33.6 L氟化氢中含有氟原子的数目为1.5 NA |
 乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4•xH2O)进行的探究性学习
乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4•xH2O)进行的探究性学习