题目内容
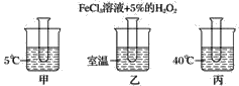
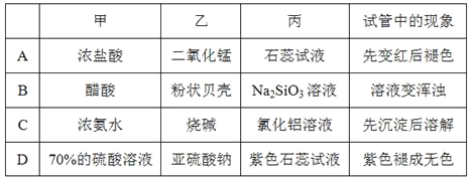
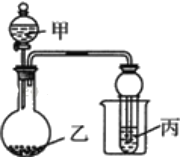
【题目】用如图所示装置进行实验,将少量液体甲逐滴加入到固体乙中,试管中试剂为丙,则下表中对应选项正确的是( )
A.A
B.B
C.C
D.D
【答案】B
【解析】
A. 二氧化锰和浓盐酸反应需要加热,该装置没有加热,所以不能产生氯气,导致不能使石蕊试液先变红后褪色,故A错误;
B. 醋酸和碳酸钙反应生成二氧化碳,二氧化碳和硅酸钠反应生成不溶于水的硅酸,所以试管中溶液变浑浊,故B正确;
C. 浓氨水和氢氧化钠混合导致氨水分解生成氨气,氨气和氯化铝反应生成氢氧化铝,虽然氢氧化铝是两性氢氧化物,但氢氧化铝不和氨水反应,所以试管中看到的现象是只生成白色沉淀,故C错误;
D. 浓硫酸和亚硫酸钠反应生成二氧化硫,二氧化硫有漂白性,但不能使酸碱指示剂褪色,所以试管中的现象是紫色变成红色,故D错误;
答案选B。

练习册系列答案
相关题目
【题目】下表是几种弱酸常温下的电离平衡常数:
CH3COOH | H2CO3 | H2S | H3PO4 |
1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
则下列说法中不正确的是( )
A. 碳酸的酸性强于氢硫酸
B. 多元弱酸的酸性主要由第一步电离决定
C. 常温下,加水稀释醋酸,![]() 增大
增大
D. 向弱酸溶液中加少量NaOH溶液,电离常数不变