题目内容
【题目】如图是某兴趣小组的探究性实验图示,有关说法合理的是( )
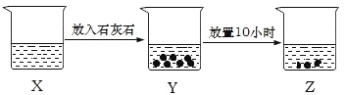
A. 若X中溶液为FeCl2溶液,则Z中最终可生成Fe(OH)2沉淀
B. 若X中溶液为新制的饱和氯水,则烧杯中液体的漂白性:X>Y>Z
C. 若X中溶液为NH4Cl溶液,则烧杯中液体的pH:X>Z
D. 若X中溶液为AlCl3溶液,可通过丁达尔现象证明 Z 中是否存在Al(OH)3胶体
【答案】D
【解析】
石灰石(CaCO3)加入,根据沉淀溶解平衡和弱电解质的电离平衡有:CaCO3(s) ![]() Ca2+(aq)+CO32-(aq),CO32-+H+
Ca2+(aq)+CO32-(aq),CO32-+H+![]() HCO3-,因此可以调节溶液的pH。
HCO3-,因此可以调节溶液的pH。
A. 若X中溶液为FeCl2溶液,FeCl2是强酸弱碱盐,Fe2+发生水解,生成Fe(OH)2白色沉淀,Fe(OH)2在空气中易被氧气氧化,则Z中最终可生成Fe(OH)3沉淀,A错误;
B. Cl2+H2O![]() H++Cl-+HClO,碳酸钙使平衡正向移动。Y中HC1O的浓度最大,z中HClO的浓度最小,所以三只烧杯液体的漂白性: Y> X> Z,故B错误;
H++Cl-+HClO,碳酸钙使平衡正向移动。Y中HC1O的浓度最大,z中HClO的浓度最小,所以三只烧杯液体的漂白性: Y> X> Z,故B错误;
C. 若X中溶液为NH4Cl溶液,X中溶液呈酸性,加入石灰石后与溶液中H+反应,溶液碱性增强,则烧杯中液体的pH:X<Z,C错误;
D. 若X中溶液为AlCl3溶液,铝离子水解形成Al(OH)3,Z 中是否存在Al(OH)3胶体,可以通过丁达尔现象证明,D正确;
答案选D。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目