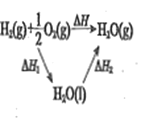题目内容
【题目】下列关于![]() 溶液的说法正确的是( )
溶液的说法正确的是( )
A.![]() 的电离方程式为:
的电离方程式为:![]()
B.![]() 时,加水稀释后,
时,加水稀释后,![]() 与
与![]() 的乘积变大
的乘积变大
C.离子浓度关系:![]()
D.![]() 时,
时,![]() 的
的![]() 溶液中,由水电离的
溶液中,由水电离的![]()
【答案】B
【解析】
A. 碳酸氢根离子为弱酸的酸式酸根离子,不能拆开;
B. 加水稀释后,促进HCO3-水解,但Kw不变;
C. 根据电荷守恒分析解答;
D. 在25℃时,水的离子积是1×10-14,盐类水解促进水的电离,据此解答。
A. 碳酸氢根离子为弱酸的酸式酸根离子,不能拆开,则NaHCO3的电离方程式为:NaHCO3 ═ Na+ + HCO3,A项错误;
B. 25℃时,加水稀释后,促进HCO3水解,n(OH)增大,但c(OH)减小,由Kw不变,可知c(H+)增大,则n(H+)增大,则n(H+)与n(OH)的乘积变大,B项正确;
C. 根据电荷守恒知,离子浓度关系应为:c(Na+)+c(H+)═c(OH)+c(HCO3)+2c(CO32),C项错误;
D. ![]() 时,pH=8的NaHCO3溶液显碱性,则HCO3的水解程度大于其电离程度,则HCO3水解会促进水的电离,溶液中c(H+)=1.0×108molL1,则溶液中c(OH)=1.0×106molL1,所以由水电离的c(OH)=1.0×106molL1,D项错误;
时,pH=8的NaHCO3溶液显碱性,则HCO3的水解程度大于其电离程度,则HCO3水解会促进水的电离,溶液中c(H+)=1.0×108molL1,则溶液中c(OH)=1.0×106molL1,所以由水电离的c(OH)=1.0×106molL1,D项错误;
答案选B。

【题目】下列实验结果不能作为相应定律或原理的证据之一的是( )
(阿伏加德罗定律:在同温同压下,相同体积的任何气体含有相同数目的分子)
A | B | C | D | |
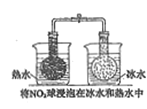
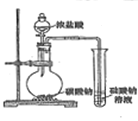
勒夏特列原理 | 元素周期律 | 盖斯定律 | 阿伏伽德罗定律 | |
实验方案 |
|
|
|
|
结果 | 左球气体颜色加深 右球气体颜色变浅 | 烧瓶中冒气泡 试管中出现浑浊 | 测得 |
|
A. AB. BC. CD. D
【题目】由![]() 羟基丁酸生成
羟基丁酸生成![]() 丁内酯的反应如下:HOCH2CH2CH2COOH
丁内酯的反应如下:HOCH2CH2CH2COOH![]() +H2O
+H2O
在298K下,![]() 羟基丁酸水溶液的初始浓度为
羟基丁酸水溶液的初始浓度为![]() ,测得
,测得![]() 丁内酯的浓度随时间变化的数据如表所示。回答下列问题:
丁内酯的浓度随时间变化的数据如表所示。回答下列问题:
| 21 | 50 | 80 | 100 | 120 | 160 | 220 |
|
| 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.116 | 0.132 |
(1)该反应在50~80min内的平均反应速率为_____![]() 。
。
(2)120min时![]() 羟基丁酸的转化率为______。
羟基丁酸的转化率为______。
(3)298K时该反应的平衡常数![]() _____。
_____。
(4)为提高![]() 羟基丁酸的平衡转化率,除适当控制反应温度外,还可采取的措施是______。
羟基丁酸的平衡转化率,除适当控制反应温度外,还可采取的措施是______。