题目内容
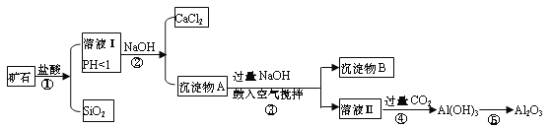
【题目】榴石矿石可以看作CaO、FeO、Fe2O3、Al2O3、SiO2组成。工业上对其进行综合利用的流程如下:
(1)用方程式表示盛放氢氧化钠溶液的试剂瓶不能用玻璃塞的原因________;
(2)溶液Ⅰ中除了Ca2+外,还可能含有的金属阳离子有_______________;
(3)步骤③中NaOH参加反应的离子方程式是________________,鼓入空气并充分搅拌的目的是_____________________。
(4)在工业生产中,步骤④通入过量CO2而不加入盐酸的原因是___________;写出步骤④通入过量CO2的离子方程式 _________________________________。
(5)试设计实验证明榴石矿中含有FeO(试剂任选,说明实验操作与现象)_________。
【答案】2 NaOH+SiO2 =Na2 SiO3 +H2OH+、Al3+、Fe3+ 、Fe2+Al (OH)3+OH-===AlO2-+2H2O使氢氧化亚铁全部转化为氢氧化铁使用二氧化碳可以避免盐酸过量导致生成的氢氧化铝溶解,同时二氧化碳容易制取且价格便宜AlO2-+2H2O + CO2 =Al (OH)3 +HCO3-取少量矿石,加稀硫酸溶解后,向其中滴加酸性的高锰酸钾溶液,若紫色退去,证明矿石中含有FeO (加盐酸溶解或取溶液Ⅰ进行实验不得分)
【解析】
榴石矿石可以看作CaO、FeO、Fe2O3、A12O3、SiO2组成,加入盐酸溶解过滤得到滤液中含氯化钙、氯化亚铁、氯化铁、氯化铝、盐酸,固体为SiO2,溶液中加入氢氧化钠反应生成氢氧化铁、氢氧化亚铁、氢氧化铝,过滤得到沉淀物A加热过量氢氧化钠通入空气,氧化氢氧化亚铁生成沉淀物氢氧化铁和溶液Ⅱ为偏铝酸钠溶液,通入过量二氧化碳生成氢氧化铝沉淀,加热分解生成氧化铝;
(1)二氧化硅是酸性氧化物和碱反应生成盐和水;
(2)溶液Ⅰ除去钙离子,含有阳离子H+、Fe2+、Fe3+、Al3+;
(3)步骤③中NaOH参加反应和氢氧化铝反应生成偏铝酸钠溶液,鼓入空气充分搅拌是为了氢氧化亚铁氧化为氢氧化铁;
(4)步骤④通入过量CO2而不加入盐酸的原因是避免盐酸过量使氢氧化铝溶解,二氧化碳制备方法简单价格便宜,过滤的二氧化碳和偏铝酸钠反应生成氢氧化铝沉淀和碳酸氢钠;
(5)取少量矿石加入稀硫酸溶解后加入高锰酸钾溶液若褪色证明含有氧化亚铁。
榴石矿石可以看作CaO、FeO、Fe2O3、A12O3、SiO2组成,加入盐酸溶解过滤得到滤液中含氯化钙、氯化亚铁、氯化铁、氯化铝、盐酸,固体为SiO2,溶液中加入氢氧化钠反应生成氢氧化铁、氢氧化亚铁、氢氧化铝,过滤得到沉淀物A加热过量氢氧化钠通入空气,氧化氢氧化亚铁生成沉淀物氢氧化铁,和溶液Ⅱ为偏铝酸钠溶液,通入过量二氧化碳生成氢氧化铝沉淀,加热分解生成氧化铝;
(1)玻璃中的二氧化硅和氢氧化钠溶液反应,生成硅酸钠和水,反应的化学方程式为:2NaOH+SiO2=Na2SiO3+H2O,
故答案为:2NaOH+SiO2=Na2SiO3+H2O;
(2)依据流程分析判断,溶液Ⅰ除去钙离子,含有阳离子Fe2+、Fe3+、Al3+,溶液ⅠpH<1,说明盐酸过量,溶液中还含有H+,
故答案为:H+、Fe2+、Fe3+、Al3+;
(3)步骤③中NaOH参加反应和氢氧化铝反应生成偏铝酸钠溶液,反应的离子方程式为:Al(OH)3+OH﹣═AlO2-+2H2O,鼓入空气充分搅拌是为了氢氧化亚铁氧化为氢氧化铁,
故答案为:Al(OH)3+OH﹣═AlO2-+2H2O;使氢氧化亚铁全部转化为氢氧化铁;
(4)步骤④通入过量CO2而不加入盐酸的原因是避免盐酸过量使氢氧化铝溶解,二氧化碳制备方法简单价格便宜,步骤④通入过量CO2的反应是二氧化碳和偏铝酸钠溶液反应生成氢氧化铝沉淀和碳酸氢钠,反应的离子方程式为:AlO2-+2H2O + CO2 =Al (OH)3 +HCO3-,
故答案为:使用二氧化碳可以避免盐酸过量导致生成的氢氧化铝溶解,同时二氧化碳容易制取且价格便宜;AlO2-+2H2O + CO2 =Al (OH)3 +HCO3-;
(5)取少量矿石,加稀硫酸溶解后,向其中滴加酸性的高锰酸钾溶液,若紫色退去,证明矿石中含有FeO,
故答案为:取少量矿石,加稀硫酸溶解后,向其中滴加酸性的高锰酸钾溶液,若紫色退去,证明矿石中含有FeO。

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案【题目】元素周期表中第三周期包括Na、Mg、Al、Si、P、S、Cl、Ar 8种元素。请回答下列问题:
(1)基态磷原子核外有________种运动状态不同的电子。
(2)第三周期8种元素按单质熔点(℃)大小顺序绘制的柱形图(已知柱形“1”代表Ar)如下所示,则其中“2”原子的结构示意图为________,“8”单质晶体的类型为________。


(3)氢化镁
储氢材料的晶胞结构如图所示,已知该晶体的密度为ρ g·cm-3,则该晶体的化学式为________,晶胞的体积为________cm3(用ρ、NA表示,其中NA表示阿伏加德罗常数的值)。
(4)实验证明:KCl、MgO、CaO三种晶体的结构与NaCl晶体的结构相似,已知NaCl、KCl、CaO晶体的晶格能数据如下表:
晶体 | NaCl | KCl | CaO |
晶格能/(kJ·mol-1) | 786 | 715 | 3 401 |
则KCl、MgO、CaO三种晶体的熔点从高到低的顺序是________________。其中MgO晶体中一个Mg2+周围和它最近且等距离的Mg2+有________个。
(5)Si、C和O的成键情况如下:
化学键 | C-O | C=O | Si-O | Si=O |
键能/(kJ·mol-1) | 360 | 803 | 464 | 640 |
C和O之间易形成含有双键的CO2分子晶体,而Si和O之间则易形成含有单键的SiO2原子晶体,请结合数据分析其原因:__________________________________________。