题目内容
(12分)
二甲醚是一种重要的清洁燃料,可替代氟利昂作制冷剂,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
(1)利用水煤气合成二甲醚的总反应为:
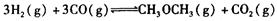
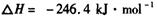
它可以分为两步,反应分别如下:
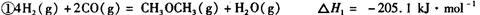

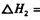 :__________________ ______________
:__________________ ______________
(2)在一定条件下的密闭容器中,该总反应达到平衡,只改变一个条件能同时提高反应速和CO的转化率的是_______(填字母代号)。
a.降低温度 b.加人催化剂 c.缩小容器体积
d.增加H2的浓度 e.增加CO的浓度
(3)在一体积可变的密闭容器中充入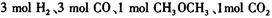 ,在一定温度和压强下发生反应:
,在一定温度和压强下发生反应: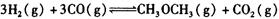 ,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:①反应开始时正、逆反应速率
,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:①反应开始时正、逆反应速率 的大小:V(正)____V(逆)(填“ >”、“ < ”或"="),理由是:________________________________
的大小:V(正)____V(逆)(填“ >”、“ < ”或"="),理由是:________________________________
②平衡时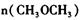 =_________________,平衡时CO的转化率= _________________。
=_________________,平衡时CO的转化率= _________________。
二甲醚是一种重要的清洁燃料,可替代氟利昂作制冷剂,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
(1)利用水煤气合成二甲醚的总反应为:
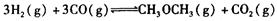
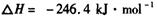
它可以分为两步,反应分别如下:
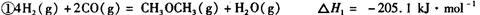

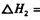 :__________________ ______________
:__________________ ______________ (2)在一定条件下的密闭容器中,该总反应达到平衡,只改变一个条件能同时提高反应速和CO的转化率的是_______(填字母代号)。
a.降低温度 b.加人催化剂 c.缩小容器体积
d.增加H2的浓度 e.增加CO的浓度
(3)在一体积可变的密闭容器中充入
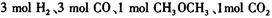 ,在一定温度和压强下发生反应:
,在一定温度和压强下发生反应: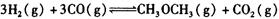 ,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:①反应开始时正、逆反应速率
,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:①反应开始时正、逆反应速率 的大小:V(正)____V(逆)(填“ >”、“ < ”或"="),理由是:________________________________
的大小:V(正)____V(逆)(填“ >”、“ < ”或"="),理由是:________________________________②平衡时
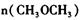 =_________________,平衡时CO的转化率= _________________。
=_________________,平衡时CO的转化率= _________________。(12分)


略

练习册系列答案
相关题目
 C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol·L-1c(B)="0.200" mol·L-1 c(C)="0" mol·L-1。反应物A的浓度随时间的变化如右图所示。
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol·L-1c(B)="0.200" mol·L-1 c(C)="0" mol·L-1。反应物A的浓度随时间的变化如右图所示。

 CH3CH2OH(g)+H2O(g)
CH3CH2OH(g)+H2O(g)
 Ur-(尿酸根,aq) + H+(aq) (37℃时,Ka =4.0×10-6)
Ur-(尿酸根,aq) + H+(aq) (37℃时,Ka =4.0×10-6)
 2NO(g)+ O2(g),能说明该反应已达化学平衡状态的是
2NO(g)+ O2(g),能说明该反应已达化学平衡状态的是 p C在某温度下达到平衡。
p C在某温度下达到平衡。 3C(g),若反应开始时充入2 mol A和2 mol B,达到平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数小于a%的是
3C(g),若反应开始时充入2 mol A和2 mol B,达到平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数小于a%的是 2TaS2(s)+2I2(g),t min后达到平衡,此时生成2a mol I2。下列说法正确的是 ( )
2TaS2(s)+2I2(g),t min后达到平衡,此时生成2a mol I2。下列说法正确的是 ( )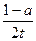 mol/(L·min)
mol/(L·min)