题目内容
由碳的氧化物直接合成乙醇燃料已进入大规模生产。下图是由二氧化碳合成乙醇的技术流程:

吸收池中盛有饱和碳酸钾溶液,把含有二氧化碳的空气吹入吸收池中,吸收池中反应液进入分解池后,向分解池中通入高温水蒸汽,把二氧化碳从溶液中提取出来,在合成塔中和氢气经化学反应使之变为可再生燃料乙醇。回答下列问题:
(1)写出吸收池中反应的离子方程式 。
(2)从分解池中循环使用的物质是 。
(3)工业上还采取以CO和H2为原料合成乙醇,其化学反应方程式为:
2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g)
CH3CH2OH(g)+H2O(g)
写出该反应的化学平衡常数表达式 K= 。
(4)在相同条件下,由CO制取CH3CH2OH的平衡常数远远大于由CO2制取CH3CH2OH的平衡常数。则由CO制取CH3CH2OH的优点是使原料有较大的转化率 ,由CO2制取CH3CH2OH的优点是 。(写出一点即可)
(5)在一定压强下,测得由CO2制取CH3CH2OH的实验数据如下表:
根据表中数据分析:
①温度升高,该反应的平衡常数K值 (选填“增大”、“减小”或“不变”);
②提高氢碳n(H2)/n(CO2)比,对生成乙醇 (选填“不利”、“有利”或“无影响”)。

吸收池中盛有饱和碳酸钾溶液,把含有二氧化碳的空气吹入吸收池中,吸收池中反应液进入分解池后,向分解池中通入高温水蒸汽,把二氧化碳从溶液中提取出来,在合成塔中和氢气经化学反应使之变为可再生燃料乙醇。回答下列问题:
(1)写出吸收池中反应的离子方程式 。
(2)从分解池中循环使用的物质是 。
(3)工业上还采取以CO和H2为原料合成乙醇,其化学反应方程式为:
2CO(g)+4H2(g)
 CH3CH2OH(g)+H2O(g)
CH3CH2OH(g)+H2O(g)写出该反应的化学平衡常数表达式 K= 。
(4)在相同条件下,由CO制取CH3CH2OH的平衡常数远远大于由CO2制取CH3CH2OH的平衡常数。则由CO制取CH3CH2OH的优点是使原料有较大的转化率 ,由CO2制取CH3CH2OH的优点是 。(写出一点即可)
 | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
根据表中数据分析:
①温度升高,该反应的平衡常数K值 (选填“增大”、“减小”或“不变”);
②提高氢碳n(H2)/n(CO2)比,对生成乙醇 (选填“不利”、“有利”或“无影响”)。
(1)CO2+CO32-+H2O==2HCO3- (3分)
(2)K2CO3 (3分)
(3)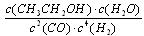 (3分)
(3分)
(4)CO2原料易得等 (3分)(其它合理答案均可给分)
(5)①减小 (2分) ②有利 (2分)
(2)K2CO3 (3分)
(3)
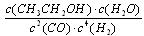 (3分)
(3分)(4)CO2原料易得等 (3分)(其它合理答案均可给分)
(5)①减小 (2分) ②有利 (2分)
略

练习册系列答案
相关题目
 2Z(气);△H=Q(Q<0)在一定条件下,反应物Y的转化率与反应时间(t)的关系如下图所示。若使曲线a变为曲线b可采取的措施是
2Z(气);△H=Q(Q<0)在一定条件下,反应物Y的转化率与反应时间(t)的关系如下图所示。若使曲线a变为曲线b可采取的措施是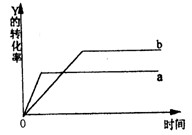
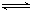 3C(g)+2D(g),(b为
3C(g)+2D(g),(b为 3的正整数) 。
3的正整数) 。 (B)= 。
(B)= 。 图所示,容器A左侧是可平行移动的活塞。向A中充入1molX和1molY,向B中充入2molX和2molY,起始时V(A)=V(B)=aL。在相同温度和有催化剂存在的条件下,两容器各自发生:X(g)+Y(g)
图所示,容器A左侧是可平行移动的活塞。向A中充入1molX和1molY,向B中充入2molX和2molY,起始时V(A)=V(B)=aL。在相同温度和有催化剂存在的条件下,两容器各自发生:X(g)+Y(g)  Z(g)+2W(g),达到平衡时V(A)=1.2aL。试回答:
Z(g)+2W(g),达到平衡时V(A)=1.2aL。试回答:
 6C + 4D
6C + 4D 2C B.A+B
2C B.A+B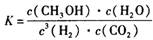 且温度升高,K值变小。下列说法正确的是
且温度升高,K值变小。下列说法正确的是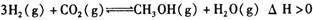
 CH3OH(g)。T1、T2温度下,CH3OH的物质的量随着时间的变化关系如下图所示。下列有关说法正确的是
CH3OH(g)。T1、T2温度下,CH3OH的物质的量随着时间的变化关系如下图所示。下列有关说法正确的是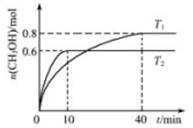
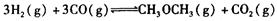
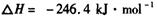
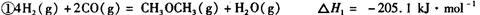

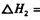 :__________________ ______________
:__________________ ______________ 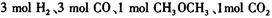 ,在一定温度和压强下发生反应:
,在一定温度和压强下发生反应: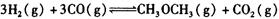 ,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:①反应开始时正、逆反应速率
,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:①反应开始时正、逆反应速率 的大小:V(正)____V(逆)(填“ >”、“ < ”或"="),理由是:________________________________
的大小:V(正)____V(逆)(填“ >”、“ < ”或"="),理由是:________________________________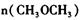 =_________________,平衡时CO的转化率= _________________。
=_________________,平衡时CO的转化率= _________________。