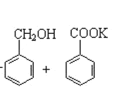
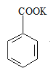
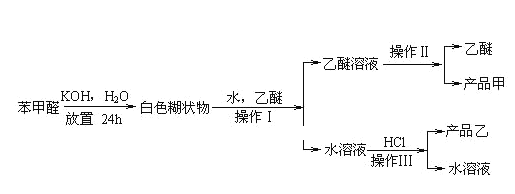
题目内容
【题目】能源开发、环境保护、资源利用等是当今社会的热门话题。请根据所学化学知识回答下列问题:
(1)汽车上安装催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
已知:N2(g) + O2(g)=2NO(g) △H=+180.5 kJ·mol-1;
2C(s)+ O2(g)=2CO(g) △H=-221.0 kJ·mol-1;
C(s)+ O2(g)=CO2(g) △H=-393.5 kJ·mol-1;
则尾气转化反应2NO(g) +2CO(g)=N2(g)+2CO2(g)的△H=________________。
(2)某硝酸厂利用甲醇处理废水。在一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32 g CH3OH转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比为______________。
(3)煤的间接液化是先转化为CO和H2,再在催化剂作用下合成甲醇。若在一定温度下,向1 L密闭容器中加入CO和H2,发生反应CO(g)+2H2(g)CH3OH(g),经10 min反应达到平衡时测得各组分的浓度如下:
物质 | CO | H2 | CH3OH |
浓度/(mol·L-1) | 1.2 | 1.0 | 0.6 |
①该反应的平衡常数表达式为:K=_____________________。
②该时间内反应速率υ(H2)=_________________。
③平衡时CO的转化率为_________________(保留1位小数)
【答案】-746.5kJ/mol 5:6 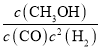 0.12mol·L-1·min-1 33.3%
0.12mol·L-1·min-1 33.3%
【解析】
(1)已知:①N2(g) + O2(g)=2NO(g) △H=+180.5 kJ·mol-1;
②2C(s)+ O2(g)=2CO(g) △H=-221.0 kJ·mol-1;
③C(s)+ O2(g)=CO2(g) △H=-393.5 kJ·mol-1;
根据盖斯定律可知③×2-①-②即得到反应2NO(g) +2CO(g)=N2(g)+2CO2(g)的![]() ;
;
(2)32g甲醇能转移6mol电子即1mol甲醇能够转移6mol电子;1mol硝酸被还原为N2,可转移5mol电子,所以还原剂和氧化剂的物质的量之比为5:6;
(3)①由反应方程式可知,该反应的平衡常数表达式为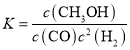 ;
;
②由反应方程式可知,10min内甲醇浓度增加0.6mol/L,那么H2浓度减少了1.2mol/L,这段时间内氢气的反应速率为![]() ;
;
③由反应方程式可知,10min内甲醇的浓度增加了0.6mol/L,那么CO的浓度减少了0.6mol/L,那么CO的转化率为![]() 。
。

 计算高手系列答案
计算高手系列答案