题目内容
7.含有非极性共价键的化合物是( )| A. | CO2 | B. | CaCl2 | C. | C2H6 | D. | NaOH |
分析 同种非金属元素之间形成非极性共价键,不同非金属元素之间形成极性共价键,以此来解答.
解答 解:A.只含有C=O键,为极性键,故A错误;
B.为离子化合物,不含共价键,故B错误;
C.含有C-C键,为非极性键,故C正确;
D.为离子化合物,含有离子键和O-H极性键,故D错误.
故选C.
点评 本题考查共价键知识,为高频考点,注意极性共价键、非极性共价键的区别以及判断方法,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
3.下列表达方式正确的是( )
| A. | 甲烷的电子式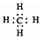 | B. | 氟化氢的电子式 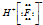 | C. | N2的电子式  | D. | Na2S的电子式  |
18.下列溶液中粒子的物质的量浓度关系正确是( )
| A. | 室温下pH=2的醋酸与pH=12的NaOH溶液等体积混合,所得溶液中:c(Na+)>c(OH)>c(CH3COO-)>c(H+) | |
| B. | 含KI、KCl均为0.1mol•L-1的混合溶液10mL与20mL0.1mol.L-1AgNO3溶液混合,所得悬浊液中:c(K+)═c(NO3-)>c(Ag+)>c(Cl-)>c(I-) | |
| C. | 室温下,向10mL0.1mol•L-1的氨水中滴加同体积同浓度的CH3COOH的溶液,在滴加过程中:$\frac{c(N{{H}_{4}}^{+)}}{c(N{H}_{3}•{H}_{2}O)}$先增大再减小 | |
| D. | CH3COONa和CaCl2混合溶液中:c(Na+)+c(Ca2+)═c(CH3COO-)+(CH3COOH)+2c(Cl-) |
2.下列各指定原子序数的元素,不能形成AB2型化合物的是( )
| A. | 6和8 | B. | 16和12 | C. | 12和9 | D. | 16和8 |
12.下列化学方程式不正确的是( )
| A. | 乙醇和浓硫酸加热至140℃反应:2CH3CH2OH$\stackrel{140℃}{→}$CH3CH2OCH2CH3+H2O | |
| B. | 溴乙烷与NaOH醇溶液加热反应:CH3CH2Br+NaOH$→_{△}^{醇}$CH2═CH2↑+NaBr | |
| C. | 苯酚钠溶液中通少量二氧化碳:C6H5O-+CO2+H2O→C6H5OH↓+HCO3- | |
| D. | 乙醛溶液与银氨溶液共热:2CH3CHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$2CH3COONH4+2Ag↓+3NH3+H2O |
19.高温下,某反应达平衡,平衡常数K=$\frac{c(CO)•c({H}_{2}O)}{c({C}_{2}O)•c({H}_{2})}$,恒容时,温度升高,H2浓度减小.下列说法正确( )
| A. | 升高温度,逆反应速率减小 | |
| B. | 恒温恒容下,增大压强,H2浓度一定减小 | |
| C. | 该反应的焓变为正值 | |
| D. | 该反应化学方程式为CO+H2O═CO2+H2 |
16.下列关于${\;}_{27}^{60}$Co原子的叙述不正确的是( )
| A. | 中子数为33 | B. | 电子数为33 | C. | 质量数为60 | D. | 质子数为27 |
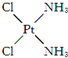 ,具有抗癌作用;反铂的结构简式为
,具有抗癌作用;反铂的结构简式为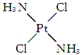 ,无抗癌作用.顺铂和反铂的物理性质有很大差异,其中只有一种易溶于水,请你通过所学知识判断哪一种易溶于水,并说明理由:顺式结构,顺铂易溶于水,因为它是极性分子,易溶于极性溶剂.
,无抗癌作用.顺铂和反铂的物理性质有很大差异,其中只有一种易溶于水,请你通过所学知识判断哪一种易溶于水,并说明理由:顺式结构,顺铂易溶于水,因为它是极性分子,易溶于极性溶剂.