题目内容
【题目】下列有关化学反应原理判断正确的是( )
A.若一定条件下,反应![]() 达平衡后,压缩容器,则反应物浓度增大,平衡正向移动
达平衡后,压缩容器,则反应物浓度增大,平衡正向移动
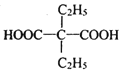
B.已知水合肼(![]() )是二元弱碱,能发生类似于多元酸的电离形式,则在水中它的第二步电离方程式为
)是二元弱碱,能发生类似于多元酸的电离形式,则在水中它的第二步电离方程式为![]()
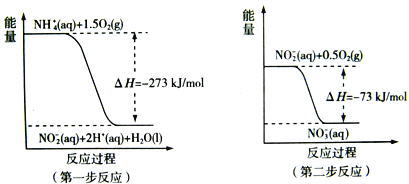
C.同温同压下,![]() 在光照和点燃条件下的
在光照和点燃条件下的![]() 不同
不同
D.在一定条件下的![]() 溶液,若升高温度,则
溶液,若升高温度,则![]() 减小
减小
【答案】B
【解析】
A.反应![]() 是一个气体系数不变的反应,达平衡后,压缩容器,则反应物浓度增大,但平衡不移动,A错误;
是一个气体系数不变的反应,达平衡后,压缩容器,则反应物浓度增大,但平衡不移动,A错误;
B.已知水合肼(![]() )是二元弱碱,能发生类似于多元酸的电离形式,第一步电离方程式为:N2H4+H2O
)是二元弱碱,能发生类似于多元酸的电离形式,第一步电离方程式为:N2H4+H2O ![]() N2H5++OH-,则在水中它的第二步电离方程式为
N2H5++OH-,则在水中它的第二步电离方程式为![]() ,B正确;
,B正确;
C.化学反应的热效应取决于反应的始终态,与反应过程无关,所以同温同压下,![]() 在光照和点燃条件下的
在光照和点燃条件下的![]() 相同,C错误;
相同,C错误;
D.CO32-+H2O![]() HCO3-+OH-,碳酸根的水解是吸热过程,所以温度升高,促进其水解,c(HCO3-)变大,c(CO32-)变小,则
HCO3-+OH-,碳酸根的水解是吸热过程,所以温度升高,促进其水解,c(HCO3-)变大,c(CO32-)变小,则![]() 变大,D错误;
变大,D错误;
答案选B。

练习册系列答案
相关题目