题目内容
【题目】在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图。又知AgCl的Ksp=1.8×10-10。下列说法不正确

A.t°C时,Ag2CrO4的Ksp为1×10-8
B.饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点
C.t°C时,Y点和Z点的Ag2CrO4的Ksp相等
D.t°C时,将0.01 mol·L-1AgNO3溶液滴入20 mL 0.01 mol·L-1KCl和0.01 mol·L-1K2CrO4的混合溶液中,Cl-先沉淀
【答案】A
【解析】
A、根据图像,Ksp=c2(Ag+)×c(CrO42-)=(1×10-3)2mol·L-1×1×10-5mol·L-1=1×10-11,故A说法错误;
B、Ag2CrO4的溶解平衡:Ag2CrO4(s)![]() 2Ag+(aq)+CrO42-(aq),加入K2CrO4,溶液中c(CrO42-)增大,c(Ag+)降低,即Y点不变为X点,故B说法正确;
2Ag+(aq)+CrO42-(aq),加入K2CrO4,溶液中c(CrO42-)增大,c(Ag+)降低,即Y点不变为X点,故B说法正确;
C、溶度积只受温度的影响,Y和Z点温度相同,溶度积相等,故C说法正确;
D、如果生成AgCl沉淀,需要c(Ag+)=![]() =1.8×10-8mol·L-1,如果生成Ag2CrO4,需要c(Ag+)=
=1.8×10-8mol·L-1,如果生成Ag2CrO4,需要c(Ag+)= ![]() =
=![]() ×10-4mol·L-1,因此先析出氯化银沉淀,故D说法正确;
×10-4mol·L-1,因此先析出氯化银沉淀,故D说法正确;
答案选A。

【题目】某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
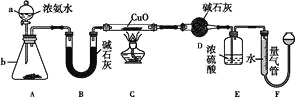
(1)仪器a的名称为____,仪器b中可选择的试剂为____。
(2)实验室中,利用装置A,还可制取的无色气体是____(填字母)。
A.Cl2 | B.O2 | C.CO2 | D.NO2 |
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体产生,上述现象证明NH3具有____性,写出相应的化学方程式:_______________________。
(4)E装置中浓硫酸的作用是_____________________________________。
(5)读取气体体积前,应对装置F进行的操作:____________________________。
(6)实验完毕,若测得干燥管D增重m g,装置F测得气体的体积为n L(已折算成标准状况),则氨分子中氮、氢的原子个数比为____(用含m、n字母的代数式表示)。