题目内容
H2S水溶液中存在电离平衡H2S H++HS-和HS-
H++HS-和HS- H++S2-若向H2S溶液中
H++S2-若向H2S溶液中
 H++HS-和HS-
H++HS-和HS- H++S2-若向H2S溶液中
H++S2-若向H2S溶液中| A.加水,平衡向右移动,溶液中氢离子浓度增大 |
| B.通入过量SO2气体,平衡向左移动,溶液pH值增大 |
| C.滴加新制氯水,平衡向左移动,溶液pH值减小 |
| D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小 |
C
加水虽平衡向正向移动,但溶液体积增大的倍数大,反而c(H+)减少,A错;通入过量的SO2虽与H2S反应,但过量生成中强酸H2SO3,溶液酸性增强,pH减少,B错;滴加新制氯水,原理几乎与通入SO2相似,C正确;加入Cu2+平衡向正方向移动,c(H+)增大,D错;答案选C。

练习册系列答案
相关题目

 和OH-
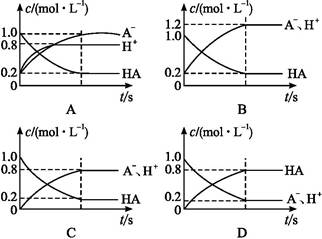
和OH- A-+H+。将1.0 mol HA分子加入水中制得1.0 L溶液,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是( )
A-+H+。将1.0 mol HA分子加入水中制得1.0 L溶液,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是( )