题目内容
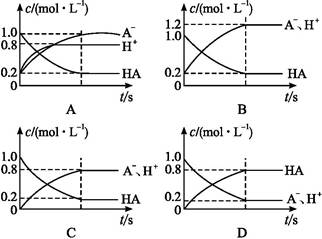
一元弱酸HA(aq)中存在下列电离平衡:HA A-+H+。将1.0 mol HA分子加入水中制得1.0 L溶液,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是( )
A-+H+。将1.0 mol HA分子加入水中制得1.0 L溶液,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是( )
 A-+H+。将1.0 mol HA分子加入水中制得1.0 L溶液,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是( )
A-+H+。将1.0 mol HA分子加入水中制得1.0 L溶液,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是( )
C
本题考查电离平衡原理与图像分析能力。根据弱酸HA的电离平衡知,HA的浓度由大到小,排除D项;A-、H+浓度由0增大,排除了A、B;平衡时,HA减小量等于A-的增加量。

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
 H++HS-和HS-
H++HS-和HS-

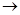 SO32— + 2HClO
SO32— + 2HClO