题目内容
盐酸、醋酸和碳酸氢钠是生活中常见的物质。下列表述正确的是( )
A.在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO 和OH- 和OH- |
| B.NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-) |
| C.10 mL0.20mol·L-1CH3COOH溶液加入10 mL0.10mol·L-1的NaOH后,溶液中:c(CH3COO-)+c(CH3COOH)= 0.10mol·L-1 |
| D.中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同 |
C
试题分析:A.在NaHCO3溶液中加入与其等物质的量的NaOH,恰好发生发生反应:NaHCO3+NaOH= Na2CO3+ H2O,得到Na2CO3。由于该盐是强碱弱酸盐。在溶液中会发生水解反应:Na2CO3+ H2O
 NaHCO3+NaOH。因此溶液中的阴离子有CO
NaHCO3+NaOH。因此溶液中的阴离子有CO 和OH-及HCO3-。错误。B.在NaHCO3溶液中:根据电荷守恒可得c(H+)+c(Na+) =c(OH-)+2c(CO
和OH-及HCO3-。错误。B.在NaHCO3溶液中:根据电荷守恒可得c(H+)+c(Na+) =c(OH-)+2c(CO )+c(HCO3-);根据物料守恒可得c(Na+)= c(CO
)+c(HCO3-);根据物料守恒可得c(Na+)= c(CO )+c(HCO3-)+c(H2CO3)。两式相减可得c(OH-)+c(CO
)+c(HCO3-)+c(H2CO3)。两式相减可得c(OH-)+c(CO )= c(H+)+c(H2CO3)。错误。C两溶液混合后得到的为等物质的量的CH3COOH与CH3COONa的混合物。根据元素守恒可得c(CH3COO-)+c(CH3COOH)= 0.10mol/L.正确。D.由于HCl是强酸,完全电离所以c(HCl)=c(H+);醋酸是弱酸,部分电离,c(CH3COOH)>> c(H+)。所以在体积与pH都相同的HCl溶液和CH3COOH溶液中含有的溶质的物质的量n(CH3COOH)>>n(HCl)因此所消耗的NaOH物质的量CH3COOH多。错误。
)= c(H+)+c(H2CO3)。错误。C两溶液混合后得到的为等物质的量的CH3COOH与CH3COONa的混合物。根据元素守恒可得c(CH3COO-)+c(CH3COOH)= 0.10mol/L.正确。D.由于HCl是强酸,完全电离所以c(HCl)=c(H+);醋酸是弱酸,部分电离,c(CH3COOH)>> c(H+)。所以在体积与pH都相同的HCl溶液和CH3COOH溶液中含有的溶质的物质的量n(CH3COOH)>>n(HCl)因此所消耗的NaOH物质的量CH3COOH多。错误。
练习册系列答案
相关题目
 L-1H2SO4洗涤Fe粉,主要反应的化学方程式为 ,之后用蒸馏水洗涤铁粉至中性;
L-1H2SO4洗涤Fe粉,主要反应的化学方程式为 ,之后用蒸馏水洗涤铁粉至中性; H++S2-
H++S2- Co2+(粉红色)+4Cl-,向氯化钴稀溶液中加入一定量的浓盐酸,溶液的颜色变化是
Co2+(粉红色)+4Cl-,向氯化钴稀溶液中加入一定量的浓盐酸,溶液的颜色变化是 H++HS-和HS-
H++HS-和HS- Na2CO3 + 2HClO
Na2CO3 + 2HClO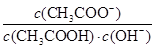 不变
不变