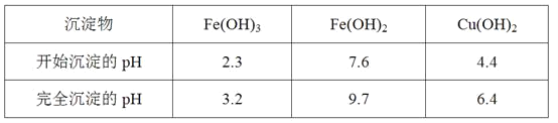
��Ŀ����
����Ŀ������ѧ����ƽ��������Ҫ��������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ��ȣ��Ҿ�������������ԭ����
һ���¶��£���1 L�ܱ������м���1 mol HI(g)��������Ӧ���й����ʵ�����ʱ��ı仯��ͼ��ʾ��
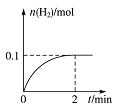
(1)0��2 min�ڵ�ƽ����Ӧ����![]() _____
_____![]() ƽ�ⳣ������ʽΪ
ƽ�ⳣ������ʽΪ![]() _________________��
_________________��
(2)��ͬ�¶��£�����ʼ����![]() �����ʵ�����ԭ����2������____��ԭ����2����
�����ʵ�����ԭ����2������____��ԭ����2����
A��ƽ�ⳣ�� B��![]() ��ƽ��Ũ��
��ƽ��Ũ��
C���ﵽƽ���ʱ�� D��ƽ��ʱ��ϵѹǿ
(3)���д�ʩ�϶���ʹƽ�����淴Ӧ�����ƶ����ǵ�_____��
A�������������� B��������0�� C�������������� D����ѹ
(4)�����£���![]() ������a L�ֱ�������������Һ��ϣ������Һ�������ԡ�
������a L�ֱ�������������Һ��ϣ������Һ�������ԡ�
�� Ũ��Ϊ![]() �İ�ˮb L����
�İ�ˮb L���� ![]() �İ�ˮc L����
�İ�ˮc L���� ![]() ������������Һd L����a��b��c��d֮���ɴ�С�Ĺ�ϵ�ǣ�_________________��
������������Һd L����a��b��c��d֮���ɴ�С�Ĺ�ϵ�ǣ�_________________��
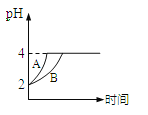
(5)�����£�ȡ![]() ������ʹ�����Һ��100 mL�������зֱ��������Zn������Ӧ����������Һ��pH�仯��ͼ��ʾ����ͼ�б�ʾ������Һ��pH�仯���ߵ���___(����A������B��)���������м����Zn����Ϊ
������ʹ�����Һ��100 mL�������зֱ��������Zn������Ӧ����������Һ��pH�仯��ͼ��ʾ����ͼ�б�ʾ������Һ��pH�仯���ߵ���___(����A������B��)���������м����Zn����Ϊ![]() ��������Һ�м����Zn����Ϊ
��������Һ�м����Zn����Ϊ![]() ����
����![]() ___
___![]() ��(ѡ������������������������)
��(ѡ������������������������)
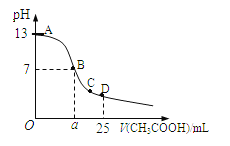
(6)ij�¶�ʱ����25mL 0.1mol/L NaOH��Һ����μ���0.2mol/L CH3COOH��Һ����������ͼ��ʾ���й�����Ũ�ȹ�ϵ�ıȽ���ȷ����____��
A����A��B����һ�㣬��Һ��һ������![]()
B����B�㣬![]() ������
������![]()
C����C�㣺![]()
D����D�㣺![]()
���𰸡�0.5��1.1 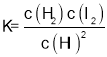 BD A b>a=d>c B < D
BD A b>a=d>c B < D
��������
����ͼ�������ƽ��״̬���������ʵ���Ϊ0.1mol�����ݷ�Ӧ����![]() ���㣬��ϻ�ѧ����ʽ��ƽ�ⳣ��������дƽ�ⳣ������ʽ����������ƽ��Ũ���ݴη��˻����Է�Ӧ��ƽ��Ũ���ݴη��˻��õ�����ͬ�¶��£�����ʼ����HI��g�������ʵ�����ԭ����2������Ӧǰ������������䣬ƽ�ⲻ�����������ʵ��������ʵ�Ũ��Ϊԭ����2����ƽ�ⳣ�����¶ȱ仯�����ݻ�ѧƽ��״̬�������ʷ�����2HI��g��H2��g��+I2��g��-Q����Ӧ�����������������ȷ�Ӧ���Ӵ�����������ʵĽǶȷ�����������Zn��Ӧͬʱ�������H+��pH�仯�ϻ�������25mL 0.1mol��L-1NaOH��Һ����μ���0.2molL-1 CH3COOH ��Һ������֮�����Ӧ����ǡ����ȫ��Ӧʱ�������������Ϊ12.5mL������Ӧ����Һ������ʱ������Ӧ�Թ�������c��OH-��=c��H+����ע����ݵ���غ�˼�����Ƚ�����Ũ�ȴ�С��
���㣬��ϻ�ѧ����ʽ��ƽ�ⳣ��������дƽ�ⳣ������ʽ����������ƽ��Ũ���ݴη��˻����Է�Ӧ��ƽ��Ũ���ݴη��˻��õ�����ͬ�¶��£�����ʼ����HI��g�������ʵ�����ԭ����2������Ӧǰ������������䣬ƽ�ⲻ�����������ʵ��������ʵ�Ũ��Ϊԭ����2����ƽ�ⳣ�����¶ȱ仯�����ݻ�ѧƽ��״̬�������ʷ�����2HI��g��H2��g��+I2��g��-Q����Ӧ�����������������ȷ�Ӧ���Ӵ�����������ʵĽǶȷ�����������Zn��Ӧͬʱ�������H+��pH�仯�ϻ�������25mL 0.1mol��L-1NaOH��Һ����μ���0.2molL-1 CH3COOH ��Һ������֮�����Ӧ����ǡ����ȫ��Ӧʱ�������������Ϊ12.5mL������Ӧ����Һ������ʱ������Ӧ�Թ�������c��OH-��=c��H+����ע����ݵ���غ�˼�����Ƚ�����Ũ�ȴ�С��
��1������ͼ�������ƽ��״̬���������ʵ���Ϊ0.1mol������HI���ʵ���Ϊ0.2mol��0��2min�ڵ�ƽ����Ӧ����![]() ����ϻ�ѧ����ʽ��ƽ�ⳣ��������дƽ�ⳣ������ʽ
����ϻ�ѧ����ʽ��ƽ�ⳣ��������дƽ�ⳣ������ʽ![]() ��
��
��2����ͬ�¶��£�����ʼ����HI��g�������ʵ�����ԭ����2������Ӧǰ������������䣬ƽ�ⲻ�����������ʵ��������ʵ�Ũ��Ϊԭ����2����ƽ�ⳣ�����¶ȱ仯��A��ƽ�ⳣ�����¶ȱ仯������Ũ�ȱ仯����A���� B����ʼ����HI��g�������ʵ�����ԭ����2������Ӧǰ������������䣬ƽ�ⲻ�����������ʵ�����HI��ƽ��Ũ��Ϊԭ����2������B��ȷ��C��Ũ������Ӧ���ʼӿ죬�ﵽƽ���ʱ����ԭ����һ�룬��C����D���������ʵ���Ϊԭ����2����ƽ��ʱ��ϵѹǿΪԭ����2������D��ȷ��
�ʴ�Ϊ��BD��
��3�����ݻ�ѧƽ��״̬�������ʷ�����2HI��g��H2��g��+I2��g��-Q����Ӧ�����������������ȷ�Ӧ��A����������������͵⻯�ⷢ����Ӧ��ƽ��������У���A��ȷ��B������ƽ������ȷ�Ӧ������У�������У����ⵥ�ʱ仯Ϊ�����ƽ��Ҳ����������Ӧ������У����̶߳ȴ�С��ͬ����ƽ���ƶ�����B����C��������������͵ⵥ�ʷ�Ӧ���ٽ�ƽ��������У���C����D����Ӧǰ������������䣬��ѹƽ�ⲻ������D����
�ʴ�Ϊ��A��
��4���ٽ�pH=3������aL��Ũ��Ϊ1.0��10-3molL-1�İ�ˮbL��Һ���ǡ�÷�Ӧ�����Ȼ����Һ��笠�����ˮ������ԣ���Һ��������Ҫ��ˮ������b��a���ڽ�pH=3������aL��c��OH-��=1.0��10-3molL-1�İ�ˮcL���������ϣ�ƽ��״̬�µ���������������Һ��������ǡ�÷�Ӧ����ʱ��ˮ����ƽ��������У�������������������Һ�����ԣ���Ҫ��������࣬a��c���۽�pH=3������aL��c��OH-��=1.0��10-3molL-1������������ҺdL��������ϣ������Ӻ�������ǡ�÷�Ӧ����Һ�����ԣ�a=d�����Եõ�b��a=d��c��
�ʴ�Ϊ��b��a=d��c��
��5�����ڴ�����������ʣ���Zn��Ӧͬʱ�������H+������pH�仯�ϻ���������B�����Ǵ�����Һ��pH�仯���ߣ���ͼ֪����ʹ����pH�仯������2��4��������������Ũ����С���������д��ڵ���ƽ�⣬�����Ӻ�п��Ӧʱ�ٽ�������룬���䷴Ӧ�������ӣ����Դ����DZ߷�Ӧ�ߵ���H+�������ĵ�Zn�࣬����m1��m2��
�ʴ�Ϊ��B������
��6��A����A��B����һ�㣬��Һ��ֻ��������������Na+��H+��CH3COO-��OH-�����ݵ���غ����У�c��Na+��+c��H+��=c��CH3COO-��+c��OH-����c��H+����c��OH-������Һ������Ũ�ȴ�С��ϵΪ��c ��Na+����c ��CH3COO-����c ��OH-����c ��H+��������ʼ���������������Һ�д�������Ũ�ȴ�С������c ��Na+����c ��OH-����c ��CH3COO-����c ��H+������A����B����B����Һ�����ԣ�������c��OH-��=c��H+�������ݵ���غ�c��Na+��+c��H+��=c��CH3COO-��+c��OH-������һ����c��Na+��=c��CH3COO-������Һ�ijɷ�Ϊ����Ӧ���ɵĴ����ƺ�ʣ��Ĵ��ᣬ�����Ƶ�ˮ��̶Ⱥʹ���ĵ���̶���ȣ����У�c��Na+��=c��CH3COO-����c��OH-��=c��H+������B����C����C�㣬��Һ�����ԣ�����c��OH-����c��H+�������ݵ���غ㣺c��Na+��+c��H+��=c��CH3COO-��+c��OH-������c��Na+����c��CH3COO-����c ��CH3COO-����c ��Na+����c ��H+����c ��OH-������C����D����D��ʱ������ʣ�࣬ʣ��Ĵ����Ũ�Ⱥ����ɵĴ�����Ũ����Ⱦ�Ϊ0.05mol/l�����������غ㣬��c��CH3COO-��+c��CH3COOH��=0.1molL-1��c��Na+��=0..05mol/L��c ��CH3COO-��+c ��CH3COOH��=2c ��Na+����D��ȷ��
�ʴ�Ϊ��D��

 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�