题目内容
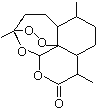
【题目】香料G的一种合成工艺如下图所示。
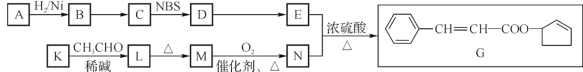
已知:A的分子式为C5H8O,它有两种不同环境的氢原子。
CH3CH2CH=CH2![]() CH3CHBrCH=CH2
CH3CHBrCH=CH2
CH3CHO+CH3CHO![]()
![]()
![]()
![]() CH3CH=CHCHO+H2O
CH3CH=CHCHO+H2O
完成下列填空:
(1)A的结构简式为________________________________。
(2)D中官能团的名称为____________________________。
(3)检验M已完全转化为N的实验操作是___________________________________________。
(4)E与浓硫酸共热可制得H,H可制备一种高分子化合物Q。写出Q的结构简式_________。
(5)写出满足下列条件的L的两种同分异构体的结构简式(不考虑立体异构):__________。
①能发生银镜反应 ②能发生水解反应 ③苯环上的一氯代物有两种
(6)以1-丁醇和NBS为原料可以制备顺丁橡胶(![]() )。请设计合成路线(其他无机原料任选)并用如下方式表示:_____________________________。
)。请设计合成路线(其他无机原料任选)并用如下方式表示:_____________________________。
![]()
【答案】![]() 碳碳双键、溴原子 取少量试样于试管中,滴加稀NaOH至溶液呈碱性,再加入新制Cu(OH)2加热至沸,若没有砖红色沉淀产生,说明M已完全转化为N
碳碳双键、溴原子 取少量试样于试管中,滴加稀NaOH至溶液呈碱性,再加入新制Cu(OH)2加热至沸,若没有砖红色沉淀产生,说明M已完全转化为N 
![]() 、
、![]() 、
、 、
、 CH3CH2CH2CH2OH
CH3CH2CH2CH2OH![]() CH3CH2CH=CH2
CH3CH2CH=CH2![]() CH3CHBrCH=CH2
CH3CHBrCH=CH2![]() CH2=CHCH=CH2
CH2=CHCH=CH2 ![]() -[-CH2CH=CHCH2-]n-
-[-CH2CH=CHCH2-]n-
【解析】
A的分子式为C5H8O,它有两种不同环境的氢原子,说明A具有对称结构,且与氢气发生加成反应,结构中含有2个不饱和结构。统观整个反应流程,K与乙醛在稀碱环境下发生反应,K含有醛基;L有醇羟基和醛基,在加热环境下发生消去反应,醇羟基转为碳碳双键;M在氧气条件下发生氧化反应,醛基氧化为羧基;N和E在浓硫酸环境下生成G,G为酯,即E含有醇羟基和五元环。通过逆推法可知,K为苯甲醛,L为C6H5-CHOH-CH2CHO,M为C6H5-CH=CH-CHO,N为C6H5-CH=CHCOOH,E为![]() ,D为
,D为![]() ,C为
,C为 ![]() ,B为环戊醇,A发生加成反应产生B,A为
,B为环戊醇,A发生加成反应产生B,A为![]() 。
。
(1)A的结构简式为![]() 。
。
(2)D为![]() ,官能团的名称为碳碳双键、溴原子。
,官能团的名称为碳碳双键、溴原子。
(3)检验M已完全转化为N,即检验醛基完全转化为羧基,无醛基结构剩余,实验操作是取少量试样于试管中,滴加稀NaOH至溶液呈碱性,再加入新制Cu(OH)2加热至沸,若没有砖红色沉淀产生,说明M已完全转化为N。
(4)E为![]() ,与浓硫酸共热可制得H,H为
,与浓硫酸共热可制得H,H为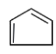 ,H制备一种高分子化合物Q, Q的结构简式为
,H制备一种高分子化合物Q, Q的结构简式为 。
。
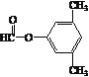
(5) L为C6H5-CHOH-CH2CHO,同分异构体①能发生银镜反应,说明含有醛基,②能发生水解反应,说明含有酯基,③苯环上的一氯代物有两种,说明苯环上取代基有两个,且取代基位于对位,或取代基有三个,但其中两个取代基结构一致,整体有机物结构存在对称轴,即同分异构体为![]() 、
、![]() 、
、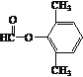 、
、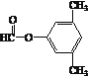 ;
;
(6)以1-丁醇和NBS为原料制备顺丁橡胶(![]() )。根据逆推法原理,顺丁橡胶的单体为1,3-丁二烯,合成路径可以为:CH3CH2CH2CH2OH
)。根据逆推法原理,顺丁橡胶的单体为1,3-丁二烯,合成路径可以为:CH3CH2CH2CH2OH![]() CH3CH2CH=CH2
CH3CH2CH=CH2![]() CH3CHBrCH=CH2
CH3CHBrCH=CH2![]() CH2=CHCH=CH2
CH2=CHCH=CH2 ![]() -[-CH2CH=CHCH2-]n-。
-[-CH2CH=CHCH2-]n-。

【题目】为测定CO2的相对分子质量,某实验小组三位同学选用含NaHCO3的样品(质量均为m1g)和其它合理的试剂,进行了以下三个实验。完成下列填空:
甲用重量法确定CO2的质量,装置如下图:
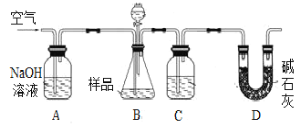
(1)B中反应的化学方程式为____________________________________________________。
(2)实验中持续缓缓通入空气,其作用之一是把生成的CO2全部排入后续装置中,使之完全被吸收;另有作用为___________________________________________________________。
(3)不能提高测定精确度的措施是___________。
a.向B内加入酸之前,排尽装置内的CO2气体
b.向B内滴加酸时不宜过快
c.在B、C之间增添盛有饱和NaHCO3溶液的洗气装置
d.在D后增添盛有碱石灰的干燥管
乙用滴定法确定CO2的物质的量,将样品配制成100mL溶液,从中取出20.00 mL,用c mol·L-1的盐酸滴定(甲基橙作指示剂)。当______________________________________________________时,停止滴定。平行测定三次,有关实验数据记录如下表。m1 g样品产生CO2的物质的量为_____________。
实验编号 | 待测液体积 (mL) | 消耗盐酸体积(mL) | |
初读数 | 末读数 | ||
1 | 20.00 | 0.00 | 25.02 |
2 | 20.00 | 0.20 | 28.80 |
3 | 20.00 | 1.30 | 26.28 |
丙用气体体积法确定CO2的体积,装置如图所示。

(4)为了减小实验误差,量气管中加入的液体X为___________________溶液;
(5)若该装置气密性良好,读数平视,但测得的“CO2体积”数据仍然偏小,其原因可能是____________________________________________________________________________。
(6)确定CO2的相对分子质量,选用___________________(限用“甲”、“乙”、“丙”进行填写)的实验数据为最佳。
【题目】某课外活动小组拟探究H+浓度对MnO2与H2O2反应速率的影响。现取等量MnO2和下表有关物质,在相同温度下进行4组实验,分别记录收集20.0mL氧气所需时间。
实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
10%H2O2的体积/mL | 5.0 | 5.0 | V1 | V2 |
20%硫酸的体积/mL | 0 | 0.5 | 1.0 | V3 |
水的体积/mL | 15 | 14.5 | V4 | 13.5 |
所需时间t/s | t1 | t2 | t3 | t4 |
已知酸性条件下时:MnO2+H2O2+2H+=Mn2++O2↑+2H2O
(1)实验Ⅰ发生反应的化学方程式为__,实验Ⅱ中MnO2的作用是__。
(2)上表中V1=__mL,V3=___mL。
(3)若实验测得t2>t3>t4,则可得出的实验结论是___。