题目内容
10.下列说法或表示方法中正确的是( )| A. | 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 由单质A转化为单质B△H=+119kJ•mol-1,可知单质B比单质A稳定 | |
| C. | 稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1 | |
| D. | 在25°C、101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ量,则表示H2燃烧热的化学方程式 2H2(g)+O2(g)═2H2O(l)△H=-571kJ•mol-1 |
分析 A、硫蒸气变化为硫固体为放热过程;
B、依据反应热量变化判断物质能量大小,物质能量越高越不稳定;
C、中和热是强酸强碱的稀溶液反应生成1mol水时放出的热量;
D、H2燃烧热是1mol氢气完全燃烧生成稳定氧化物放出的热量.
解答 解:A、硫蒸气变化为硫固体为放热过程,则等量的硫蒸气和硫固体在氧气中分别完全燃烧,放出热量硫蒸气多,故A错误;
B、由单质A转化为单质B,△H=+119kJ/mol,反应吸热,B的能量高于A,可知A比B稳定,故B错误;
C、中和热是强酸强碱的稀溶液反应生成1mol水时放出的热量,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1,故C正确;
D、在101kPa时,2gH2完全燃烧,生成液态水,放出285.8KJ热量,则氢气燃烧的热化学方程式表示为:H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8KJ/mol,故D错误;
故选C.
点评 本题考查了反应热量变化,热化学方程式的正误判断,物质能量与稳定性的比较方法,题目难度中等.

练习册系列答案
相关题目
20.下列几组顺序排列不正确的是( )
| A. | 沸点高低:HI>HBr>HCl>HF | |
| B. | 热稳定性大小:HF>H2O>NH3>PH3 | |
| C. | 熔点高低:金刚石>食盐>金属钠>冰 | |
| D. | 微粒半径大小:S2->Cl->F->Na+>Al3+ |
1.下列说法中正确的是( )
| A. | 有机物不一定都不溶于水 | |
| B. | 有机物都是共价化合物 | |
| C. | 有机物都是从有机体中分离出来的物质 | |
| D. | 有机物不具备无机物的性质 |
18.生活中遇到的某些问题,常常涉及到化学知识,下列各项叙述不正确的是( )
| A. | 鱼虾会产生不愉快的腥臭味,可在烹调时加入少量食醋和料酒 | |
| B. | “酸可以除锈”,“汽油可以去油污”都是发生了化学变化 | |
| C. | 被蜂蚁蜇咬会感觉疼痛难忍,这是由于人的皮肤被注入了甲酸的缘故,此时若能涂抹稀氨水或碳酸氢钠溶液,可以减轻疼痛 | |
| D. | 苯酚溶液可用于环境消毒,医用酒精可用于皮肤消毒 |
15.在50mL FeCl3和CuCl2的混合溶液中,FeCl3和CuCl2的浓度均为1mol/L,在混合溶液中加入100mL NaOH溶液,恰好完全反应,则该NaOH溶液的浓度为( )
| A. | 0.5mol/L | B. | 1mol/L | C. | 1.25mol/L | D. | 2.5mol/L |
19.请回答下列问题:
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
则该元素是Al(填写元素符号).
(2)基态锗(Ge)原子的价层电子排布式是4s24p2.Ge的最高价溴化物分子式是GeBr4.该元素可能的性质或应用有BD.
A.是一种活泼的金属元素 B.其单质可作为半导体材料
C.其元素的电负性大于硫元素 D.其最高价氯化物的沸点低于其溴化物的沸点
(3)关于化合物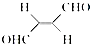 ,下列叙述正确的有AD.
,下列叙述正确的有AD.
A.该分子在水中的溶解度大于2-丁烯
B.分子中只有极性键
C.分子中有7个σ键和1个π键
D.该化合物既能发生还原反应又能发生氧化反应
E.分子间可形成氢键
(4)NaF的熔点>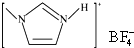 的熔点(填“>”、“=”或“<”),其原因是
的熔点(填“>”、“=”或“<”),其原因是
两者均为离子化合物,且阴阳离子电荷数均为1,但后者的离子半径较大,离子键较弱,因此其熔点较低.
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一.1molNH4BF4含有2mol配位键.
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
| 电离能 | I1 | I2 | I3 | I4 | … |
| Ia/kJ•mol-1 | 578 | 1 817 | 2 745 | 11 578 | … |
(2)基态锗(Ge)原子的价层电子排布式是4s24p2.Ge的最高价溴化物分子式是GeBr4.该元素可能的性质或应用有BD.
A.是一种活泼的金属元素 B.其单质可作为半导体材料
C.其元素的电负性大于硫元素 D.其最高价氯化物的沸点低于其溴化物的沸点
(3)关于化合物
 ,下列叙述正确的有AD.
,下列叙述正确的有AD.A.该分子在水中的溶解度大于2-丁烯
B.分子中只有极性键
C.分子中有7个σ键和1个π键
D.该化合物既能发生还原反应又能发生氧化反应
E.分子间可形成氢键
(4)NaF的熔点>
 的熔点(填“>”、“=”或“<”),其原因是
的熔点(填“>”、“=”或“<”),其原因是两者均为离子化合物,且阴阳离子电荷数均为1,但后者的离子半径较大,离子键较弱,因此其熔点较低.
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一.1molNH4BF4含有2mol配位键.



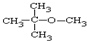 .
.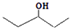 ,乙所含官能团的名称为羟基.
,乙所含官能团的名称为羟基.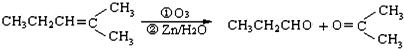
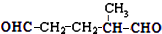 ,则烃A的结构可表示为
,则烃A的结构可表示为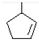 .
.