题目内容
1.下列说法中正确的是( )| A. | 有机物不一定都不溶于水 | |
| B. | 有机物都是共价化合物 | |
| C. | 有机物都是从有机体中分离出来的物质 | |
| D. | 有机物不具备无机物的性质 |
分析 A.大多数有机物不能溶于水,有的能溶;
B.CH3COONa、CH3COONH4等属于离子化合物;
C.无机物可制取有机物,尿素就是第一种由无机物制成的有机物,再如CO、H2制CH3OH;
D.无机物与有机物之间没有绝对界限.
解答 解:A.大多数有机物不能溶于水,有的能溶,比如乙醇、乙酸等有机物能溶于水,故A正确;
B.有机物不全是共价化合物,有些有机盐如CH3COONa、CH3COONH4等属于离子化合物,故B错误;
C.有机物不一定要从有机体中分离出来,如用无机物可制取有机物:CO+2H2催化剂_高温高压CH3OH(甲醇),故C错误;
D.无机物与有机物没有绝对界限,必然有某些共同特点与性质,如有机物乙酸易溶于水,无机物氯化氢也易溶于水,故D错误;
故选A.
点评 本题考查学生有关有机物和无机物的概念,可以根据所学知识来回答,题目比较简单.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
11.下列关于离子检验的说法中,正确的是( )
| A. | 向某溶液中加入澄清石灰水,溶液变浑浊,则该溶液一定含有CO32- | |
| B. | 向某溶液中加入AgNO3溶液,生成白色沉淀,该溶液中一定含有Cl- | |
| C. | 向某溶液中加入盐酸酸化的BaCl2溶液,有白色沉淀生成,该溶液中一定含有SO42- | |
| D. | 向某溶液中加入2滴KSCN溶液,溶液不显红色,再向溶液中几滴新制的氯水,溶液变为红色,该溶液中一定含有Fe2+ |
12.下列事实与氢键有关的是( )
①NH3的熔、沸点比ⅴA族相邻元素氢化物的熔、沸点高
②I2易溶于CCl4
③HF、HCl、HBr、HI的热稳定性依次减弱
④邻羟基苯甲酸的熔、沸点比对甲基苯甲酸的熔、沸点低
⑤水加热到很高的温度都难以分解
⑥CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高
⑦水结成冰体积膨胀.
①NH3的熔、沸点比ⅴA族相邻元素氢化物的熔、沸点高
②I2易溶于CCl4
③HF、HCl、HBr、HI的热稳定性依次减弱
④邻羟基苯甲酸的熔、沸点比对甲基苯甲酸的熔、沸点低
⑤水加热到很高的温度都难以分解
⑥CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高
⑦水结成冰体积膨胀.
| A. | ①②④⑥⑦ | B. | ①④⑤⑦ | C. | ①④⑦ | D. | ②③⑦ |
16.下列叙述不正确的是( )
| A. | C2H4O和C3H6O均满足饱和一元醛的通式,因此它们一定互为同系物 | |
| B. | 乙烯和苯均可使溴水褪色,但是其褪色原理不同 | |
| C. | 乙烯和苯分子中各原子都在同一平面 | |
| D. | 检验乙烷中是否含有乙烯,试剂为酸性高锰酸钾溶液 |
6.在元素周期表中,磷元素的某些信息如图所示.下列说法不正确的是( )
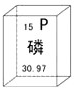

| A. | 磷元素为非金属元素 | B. | 磷原子核外有15个电子 | ||
| C. | 磷的原子序数为15 | D. | 相对原子质量为30.97g |
13.下列物质中的n等于4时,其同类别的同分异构体数目最多的是( )
| A. | 烃CnH2n+2 | B. | 醇CnH2n+2O | C. | 醛CnH2nO | D. | 羧酸CnH2nO2 |
10.下列说法或表示方法中正确的是( )
| A. | 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 由单质A转化为单质B△H=+119kJ•mol-1,可知单质B比单质A稳定 | |
| C. | 稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1 | |
| D. | 在25°C、101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ量,则表示H2燃烧热的化学方程式 2H2(g)+O2(g)═2H2O(l)△H=-571kJ•mol-1 |

