题目内容
【题目】大气中硫、氮的氧化物是形成酸雨的主要物质。某地酸雨中可能含有下列离子:Na+、Ba2+、NH4+、Al3+、Cl-、SO32-、SO42-、NO3-等。某研究小组取该地一定量的酸雨,浓缩后将所得澄清试液分成三份,进行如下实验:
试样 | 所加试剂 | 实验现象 |
第一份试液 | 滴加适量的淀粉KI溶液 | 溶液呈蓝色 |
第二份试液 | 滴加用盐酸酸化的BaCl2溶液 | 有白色沉淀产生 |
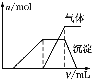
第三份试液 | 滴加NaOH溶液,加热,加入的NaOH溶液体积(V)与生成的沉淀、产生的气体的物质的量(n)的关系如图 |
|
请回答下列问题:
(1)根据实验结果判断该酸雨中肯定不存在的离子是____,不能确定的离子有___。
(2)写出第一份试液滴加淀粉KI溶液时发生反应的离子方程式:____。
(3)第三份试液滴加NaOH溶液,加热,整个过程中发生了多个反应,写出其中两个反应的离子方程式:
①最初发生的离子反应____。
②最后发生的离子反应____。
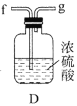
(4)该小组为了探究NO参与硫酸型酸雨的形成过程,在烧瓶中充入含有少量NO的SO2气体,再慢慢通入O2,发生化学反应后,再喷洒适量蒸馏水即得硫酸型酸雨,则NO在上述反应中的作用是_____。
【答案】SO32-、Ba2+ Na+、Cl- 6I-+2NO3-+8H+=2NO↑+3I2+4H2O H++OH-=H2O Al(OH)3+OH-=AlO2-+2H2O 催化剂
【解析】
第一份试液:滴加适量的淀粉KI溶液,显示蓝色,证明一定含有能将碘离子氧化的氧化性离子,因NO3-单独存在氧化性很弱,所以一定会含有H+和NO3-,一定不含有SO32-,因为亚硫酸根离子具有强的还原性,易被氧化,酸性条件下和硝酸根离子不能共存;
第二份试液:滴加用盐酸酸化BaCl2溶液,出现白色沉淀,则一定含有SO42-,和硫酸根离子反应的Ba2+一定不存在;
第三份试液:滴加NaOH溶液,加热,加入的NaOH溶液,产生气体,一定是氨气,所以一定含有NH4+,加入氢氧化钠产生沉淀,继续滴加氢氧化钠,沉淀会消失,所以一定含有Al3+;钠离子和氯离子是否存在不能判断;
(3)氢氧根可以和氢离子发生中和反应,可以和铝离子发生反应,可以和铵根离子发生反应,结合图像,根据混合溶液中复分解反应先后顺序分析;
(4)根据物质的性质来书写方程式,根据一氧化氮在反应中的特点来判断所起到的作用。
(1)根据上述分析,知道酸雨中肯定不存在的离子是SO32-、Ba2+,Na+、Cl-是否存在不能确定;
(2)试液中滴加淀粉KI溶液后,硝酸的存在会将碘离子氧化为碘单质,发生的反应为:6I-+2NO3-+8H+=2NO↑+3I2+4H2O;
(3)第三份试液滴加NaOH溶液,加热整个过程中有多个反应,根据分析中存在的离子,结合图像,第一个发生的反应为:氢氧根离子与氢离子反应,离子反应为:H++OH-=H2O;最后发生的是氢氧化铝和氢氧化钠反应生成偏铝酸钠和水,离子反应为:Al(OH)3+OH-=AlO2-+2H2O;
(4)一氧化氮具有还原性,很容易被氧化,氧化后产物是二氧化氮,2NO+O2=2NO2,二氧化氮还可以将二氧化硫氧化,即NO2+SO2=SO3+NO,整个过程中,一氧化氮的质量没有发生变化,起到催化剂的作用。

 步步高达标卷系列答案
步步高达标卷系列答案【题目】某研究性学习小组为了探究醋酸的电离情况,进行了如下实验:
(1)取冰醋酸配制250 mL 0.4 mol·L-1的醋酸溶液,用0.4 mol·L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
①将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如右图所示。则稀释过程中溶液的pH由大到小的顺序______(填字母)。

②配制250 mL 0.4 mol·L-1 醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和____________。
③为标定该醋酸溶液的准确浓度,用0.2000 mol·L-1的NaOH溶液对20.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
该醋酸溶液的准确浓度为_____________(保留小数点后四位),上述标定过程中,造成测定结果偏高的原因可能是_______________(多选、错选不得分)。
a.未用标准液润洗碱式滴定管
b.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
c.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
d.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
(2)该小组同学探究浓度对醋酸电离程度的影响时,用pH计测定25℃时不同浓度的醋酸的pH,其结果如下:
醋酸浓度( mol·L-1) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
①根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是______________________________________________________________。
②简述用pH试纸测 0.1mol·L-1 醋酸溶液pH的方法___________。
③利用水解理论设计实验证明醋酸的酸性比碳酸的强:______________________。