题目内容
【题目】请根据所学化学反应原理,解决以下问题:
(1)依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池,可以提供稳定的电流.装置如图所示,其中盐桥中装有琼脂-饱和KCl溶液。
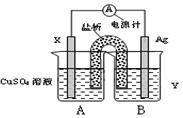
回答下列问题:
①电极X的材料和电解质溶液Y分别为________、________;
②盐桥中K+移向________(填A或B);
③银电极发生的电极反应式为________;
④该电池工作时,假设电路中有0.1mol电子转移,则X电极质量改变量为________克。
(2)已知:C(s)+O2(g)═CO2(g) △H1=-396.5kJmol-1;
H2(g)+![]() O2═H2O(g) △H2=-241.8kJmol-1;
O2═H2O(g) △H2=-241.8kJmol-1;
CO(g)+![]() O2(g)═CO2(g) △H3=-283.0kJmol-1.
O2(g)═CO2(g) △H3=-283.0kJmol-1.
根据盖斯定律写出单质碳和水蒸气生成水煤气的热化学方程式:________。
【答案】Cu AgNO3溶液 B Ag++e-=Ag 3.2 C(s)+H2O(g)=CO(g)+H2(g) △H=+128.3kJmol-1;
【解析】
(1)①氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)中失电子的金属Cu为负极,得电子的阳离子Ag+是电解质中的阳离子,所以电解质可以选择AgNO3溶液;
②原电池反应,B池中Ag+析出,为满足溶液的电中性,盐桥中的钾离子移向B池;
③银电极发生的电极反应为溶液中的银离子得到电子析出银单质,电极反应为:Ag++e-=Ag;
④铜电极是负极,电极反应式为Cu-2e-=Cu2+,该电池工作时,假设电路中有0.1mol电子转移,则X电极质量改变量为0.05mol×64g/mol=3.2g;
(2)已知:①已知:C(s)+O2(g)=CO2(g)△H1=-396.5kJmol-1
②H2(g)+![]() O2(g)=H2O(g)△H2=-241.8kJmol-1
O2(g)=H2O(g)△H2=-241.8kJmol-1
③CO(g)+![]() O2(g)=CO2(g)△H3=-283.0kJmol-1
O2(g)=CO2(g)△H3=-283.0kJmol-1
根据盖斯定律,①-②-③得到:单质碳和水蒸气生成水煤气的热化学方程式:C(s)+H2O(g)=CO(g)+H2(g) △H=+128.3kJmol-1。

【题目】大气中硫、氮的氧化物是形成酸雨的主要物质。某地酸雨中可能含有下列离子:Na+、Ba2+、NH4+、Al3+、Cl-、SO32-、SO42-、NO3-等。某研究小组取该地一定量的酸雨,浓缩后将所得澄清试液分成三份,进行如下实验:
试样 | 所加试剂 | 实验现象 |
第一份试液 | 滴加适量的淀粉KI溶液 | 溶液呈蓝色 |
第二份试液 | 滴加用盐酸酸化的BaCl2溶液 | 有白色沉淀产生 |
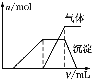
第三份试液 | 滴加NaOH溶液,加热,加入的NaOH溶液体积(V)与生成的沉淀、产生的气体的物质的量(n)的关系如图 |
|
请回答下列问题:
(1)根据实验结果判断该酸雨中肯定不存在的离子是____,不能确定的离子有___。
(2)写出第一份试液滴加淀粉KI溶液时发生反应的离子方程式:____。
(3)第三份试液滴加NaOH溶液,加热,整个过程中发生了多个反应,写出其中两个反应的离子方程式:
①最初发生的离子反应____。
②最后发生的离子反应____。
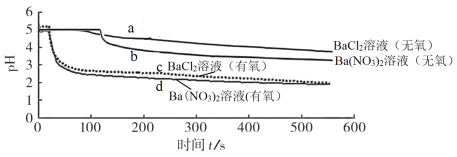
(4)该小组为了探究NO参与硫酸型酸雨的形成过程,在烧瓶中充入含有少量NO的SO2气体,再慢慢通入O2,发生化学反应后,再喷洒适量蒸馏水即得硫酸型酸雨,则NO在上述反应中的作用是_____。