题目内容
【题目】常温下,在由水电离产生的H+浓度为1x1013 mol/L 的溶液中,一定能大量共存的离子组是
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
【答案】D
【解析】试题分析:常温下,在由水电离产生的H+浓度为1x1013 mol/L 的溶液中,水的电离受到了强酸或强碱的抑制,溶液可能显酸性,也可能显碱性。A. ![]() 等4种离子中,在酸性条件下,硝酸根离子可以把亚铁离子氧化而不能大量共存,亚铁离子在强碱性条件下也不能大量存在;B.
等4种离子中,在酸性条件下,硝酸根离子可以把亚铁离子氧化而不能大量共存,亚铁离子在强碱性条件下也不能大量存在;B. ![]() 等4种离子中,镁离子在碱性条件下不能大量存在;C.碳酸氢根离子既不能大量存在于强酸性溶液也不能大量存在于强碱性溶液;D.
等4种离子中,镁离子在碱性条件下不能大量存在;C.碳酸氢根离子既不能大量存在于强酸性溶液也不能大量存在于强碱性溶液;D. ![]() 等4种离子不论在酸性溶液还是在碱性溶液中,都不能发生离子反应。综上所述,一定能大量共存的离子组是D,本题选D。
等4种离子不论在酸性溶液还是在碱性溶液中,都不能发生离子反应。综上所述,一定能大量共存的离子组是D,本题选D。

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案【题目】某学习小组研究NaOH与某些酸之间的反应。
Ⅰ.中和热的测定
在25℃、101kPa条件下,强酸与强碱的稀溶液中和热可表示为:H+(aq)+OH─(aq)=H2O(l) △H=-57.3kJ ·mol-1。按照图1所示装置进行实验。
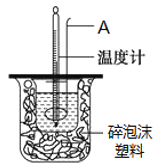
(1)仪器A的名称是________。
(2)碎泡沫塑料的作用是________。
(3)在25℃、101kPa条件下,取50mL 0.50 mol·L-1 CH3COOH溶液、50mL 0.55 mol·L-1 NaOH溶液进行实验,测得的中和热△H________-57. 3 kJ ·mol-1(填“>”“=”或“<”),原因是 ________。
Ⅱ.中和滴定
(1)用_______量取20.00 mL待测稀盐酸溶液放入锥形瓶中,并滴加1~2滴酚酞作指示剂,用0.20 mol·L—1NaOH标准溶液进行滴定。为了减小实验误差,该同学一共进行了三次实验,假设每次所取稀盐酸体积均为20.00 mL,三次实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗NaOH溶液体积/mL | 19.00 | 23.00 | 23.02 |
该盐酸的浓度约为________ (保留两位有效数字)。滴定达到终点的标志是________。
(2)若某次滴定结束时,滴定管液面如图2所示,则终点读数为________mL。