题目内容
【题目】在托盘天平的两盘上各放一只质量相同的烧杯,在两只烧杯里分别加入等质量、等溶质质量分数的稀硫酸,将天平调节至平衡。然后向左盘的烧杯中加入8.4g铁,反应物之间恰好完全反应。欲使天平恢复平衡,则可向右盘的烧杯中加入( )
A.8.4g碳酸钠B.8.4g氧化钙C.8.4g镁D.8.4g碳酸镁
【答案】C
【解析】
根据反应:
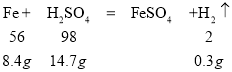
8.4 g铁产生氢气0.3 g,溶液增加的质量=8.4 g-0.3 g=8.1 g,欲使天平恢复平衡,那么右盘增加的质量也应该为8.1 g。铁与硫酸恰好完全反应,可得m(H2SO4)=14.7g。
A.碳酸钠与硫酸反应的化学方程式:
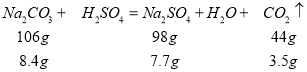
溶液实际增加的质量=8.4 g-3.5 g=4.9 g,不会平衡,选项A错误;
B.CaO+H2O=Ca(OH)2,质量增加8.4 g ,不会平衡,选项B错误;
C. 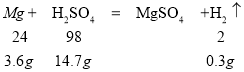
此反应中金属镁过量,生成了0.3 g的氢气,溶液增加的质量为8.4 g-0.3 g=8.1 g ,天平平衡,选项C正确;
D.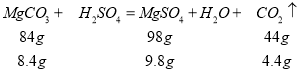
溶液实际增加的质量=8.4 g-4.4 g=4 g,天平不会平衡,选项D错误。
答案选C。

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目