题目内容
下列叙述正确的是
| A.0.1mol・L-1CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B.NH4Cl溶液加水稀释后,恢复至原温度,pH和KW均增大 |
| C.pH=4的CH3COOH溶液和pH=4的NH4Cl溶液中,c(H+)不相等 |
| D.在NaHCO3溶液中:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
D
解析试题分析:A、因为CH3COO?水解式溶液呈碱性,所以0.1mol・L-1CH3COONa溶液中离子浓度:c(Na+)>c(CH3COO-)>c(OH-)>c(H+),错误;B、温度不变,KW不变,错误;C、pH相等,说明溶液中H+浓度相等,错误;D、在NaHCO3溶液中,存在三个平衡:H2O 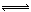 H++OH?,HCO3?
H++OH?,HCO3?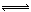 CO32?+H+,HCO3?+H2O
CO32?+H+,HCO3?+H2O 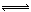 H2CO3+OH?,所以c(OH-)+c(CO32-)=c(H+)+c(H2CO3),正确。
H2CO3+OH?,所以c(OH-)+c(CO32-)=c(H+)+c(H2CO3),正确。
考点:本题考查离子浓度比较。

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-12。某溶液中含有Cl-、Br-和CrO42-,浓度均为0.010mol?L-1,向该溶液中逐滴加入0.010 mol?L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
| A.Cl-、Br-、CrO42- | B.CrO42-、Br-、Cl- | C.Br-、Cl-、CrO42- | D.Br-、CrO42-、Cl- |
下列溶液中粒子的物质的量浓度关系正确的是
| A.0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中: c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) |
| B.20ml0.1mol/LCH3COONa溶液与10ml0.1mol/LHCl溶液混合后呈酸性,所得溶液中: c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
| C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中: c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| D.0.1mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中: |
已知某温度下CH3COOH和NH3?H2O 的电离常数相等,现向10mL浓度为0.1mol?L?1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中
| A.水的电离程度始终增大 |
| B.c(NH4+)/c(NH3?H2O)先增大再减小 |
| C.c(CH3COOH)与c(CH3COO?)之和始终保持不变 |
| D.当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO?) |
下列叙述中正确的是
| A.二氧化氯具有还原性,可用于自来水的杀菌消毒 |
| B.碳酸钠溶液呈碱性,医疗上常用碳酸钠治疗胃酸过多 |
| C.向纯水中加入盐酸或降温都能使水的离子积减小,电离平衡逆向移动 |
| D.锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后,再将不溶物用稀盐酸溶解去除 |
由几种常见的盐混合组成的白色粉末,其中只可能含有Na+、K+、Al3+、CO32-、HCO3-、SO42-、NO2-中的若干种离子。某同学对该溶液进行如下实验:
以下说法正确的是
| A.白色沉淀甲是Al(OH)3,气体甲是CO2,所以混合物一定含Al3+和HCO3- |
| B.气体乙一定是NO和NO2的混合气体 |
| C.白色沉淀乙是BaSO4,所以原混合物一定含有SO42- |
| D.白色粉末中一定含有Na+ 、Al3+ 、NO2- |
HF为一元弱酸,在0.1mol・L-1 NaF溶液中,离子浓度关系正确的是
| A.c(Na+)>c(F-)>c(H+)>c(OH-) | B.c(Na+)>c(OH-)>c(F-)>c(H+) |
| C.c(Na+) + c(OH-)=c(F-) + c(H+) | D.c(Na+) + c(H+)=c(F-) + c(OH-) |
下列有关实验的叙述正确的是
| A.已知Cu2O+2H+=Cu2++Cu+H2O,氢气还原氧化铜后生成的红色固体能完全溶于稀硝酸,说明还原产物是铜 |
| B.在中和热测定的实验中,将NaOH溶液和盐酸混合反应后的冷却温度作为末温度 |
| C.仅用淀粉溶液、稀硫酸、碘水、新制氢氧化铜四种试剂可完成淀粉水解产物及水解程度检验的探究实验 |
| D.向盛有少量Mg(OH )2悬浊液的试管中滴加氯化铵溶液,可以看到沉淀溶解 |