题目内容
下列叙述中正确的是
| A.二氧化氯具有还原性,可用于自来水的杀菌消毒 |
| B.碳酸钠溶液呈碱性,医疗上常用碳酸钠治疗胃酸过多 |
| C.向纯水中加入盐酸或降温都能使水的离子积减小,电离平衡逆向移动 |
| D.锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后,再将不溶物用稀盐酸溶解去除 |
D
解析试题分析:A、二氧化氯具有氧化性,用于自来水的杀菌消毒,错误;B、碳酸钠溶液的碱性比碳酸氢钠溶液的碱性强,所以医疗上常用碳酸氢钠治疗胃酸过多,错误;C、加入盐酸,温度不变,所以水的离子积不变,错误;D、碳酸钙的溶解度比硫酸钙的溶解度小,所以锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后,硫酸钙转化为碳酸钙,然后碳酸钙与稀盐酸反应生成易溶的氯化钙除去,正确,答案选D。
考点:考查生活中的化学应用,水的离子积的变化,锅炉除垢的原理

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
25℃时,下列溶液中水的电离程度最小的是
| A.0.01 mol/L盐酸 | B.0.01 mol/L Na2CO3溶液 |
| C.pH =" 4" NaHSO3溶液 | D.pH =11氨水 |
下列说正确的是
【已知:HClO的Ka=3.0×l0-8;H2CO3的Ka1= 4.3×l0-7,Ka2=5.6×l0-11;Ksp(BaSO4)=" 1.1" ×10-10;Ksp(BaCO3)=" 5.1" ×10-9】
| A.相同条件下,pH相同的NaClO和Na2CO3溶液,物质的量浓度前者小于后者 |
| B.常温下,将CH3COONa溶液和稀盐酸混合至溶液pH=7时: c(Na+)>c(CH3COO-)>c(Cl-) >c(CH3COOH)>c(H+)=c(OH-) |
| C.向饱和Na2CO3溶液中通入足量的CO2,溶液变浑浊,由此证明了NaHCO3溶解度比Na2CO3小 |
| D.氯碱工业使用的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。除杂时,粗盐水中可先加入过量的BaCl2溶液,至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后滤去沉淀,所得滤液中仍含有一定量的SO42- |
下列关于0.10 mol·L-1 NaHCO3溶液的说法正确的是
| A.溶质的电离方程式为NaHCO3=Na++ H++ CO32- |
| B.25 ℃时,加水稀释后,n(H+)与n(OH-)的乘积变大 |
| C.离子浓度关系:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
| D.温度升高,c(HCO3-)增大 |
室温下,甲、乙两烧杯均盛有5mlpH=3的某一元酸溶液,向乙烧杯中加水稀释至pH=4,关于甲、乙两烧杯中溶液的描述正确的是
| A.溶液的体积:10V甲≤V乙 |
| B.水电离出的OH-浓度:10c(OH-)甲≤c(OH-)乙 |
| C.若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙 |
| D.若分别与5mlpH=11的NaOH溶液反应,所得溶液的pH:甲≤乙 |
下列叙述正确的是
| A.0.1mol·L-1CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B.NH4Cl溶液加水稀释后,恢复至原温度,pH和KW均增大 |
| C.pH=4的CH3COOH溶液和pH=4的NH4Cl溶液中,c(H+)不相等 |
| D.在NaHCO3溶液中:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
下列叙述正确的是 ( )
| A.将过量CO2气体通入水玻璃中可制得硅酸和纯碱 |
B.标准状况下,2.24L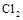 与过量稀NaOH溶液反应,转移电子0.1mol 与过量稀NaOH溶液反应,转移电子0.1mol |
| C.1L2mol·L-1明矾经水解可得到氢氧化铝胶体粒子数目为2×6.02×1023 |
| D.漂白粉溶于水能导电,故漂白粉是电解质 |
相同温度,浓度均为0.1mol /L,等体积的三种溶液:①HF溶液、②CH3COOH溶液、③NaHCO3溶液,已知将①、②分别与③混合,实验测得产生的CO2气体体积(v)随时间(t)的变化如右图所示,下列说法正确的是( )
| A.上述三种溶液中:c( OH-)大小:③ > ② > ① |
| B.物质酸性的比较:CH3COOH > HF > H2CO3 |
| C.反应结束后所得两溶液中: c ( CH3COO- ) > c ( F- ) |
| D.①和③反应结束后所得溶液中:c ( F- ) + c (HF) =" 0.10mol" /L |