题目内容
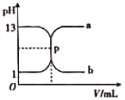
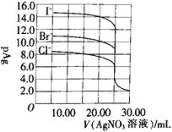
【题目】体积和浓度均为25.00mL0.1mol/LNaI、NaBr及NaCl三种溶液,分别用0.1mol/L的AgNO3溶液滴定,滴定曲线如图所示[pAg=-lgc(Ag+)]。下列说法不正确的是( )
A.Ksp(AgI)<Ksp(AgBr)<Ksp(AgCl)
B.AgNO3溶液滴定Cl-时,可加入少量的KI作滴定指示剂
C.三种溶液等体积等浓度混合后用AgNO3溶液滴定,沉淀顺序为I-、Br-、Cl-
D.当V(AgNO3)=30.00mL时,三种溶液中:c(I-)<c(Br-)<c(Cl-)
【答案】B
【解析】
A.由图象可知,滴加AgNO3溶液10.00mL时,AgNO3少量,溶液中c(Ag+)按I-、Br-、Cl-依次增大,故Ksp(AgI)<Ksp(AgBr)<Ksp(AgCl),A正确;
B.滴加硝酸银滴定Cl-时,若用KI作为指示剂,I-优先与Ag+反应生成沉淀,故不能用KI作为滴定指示剂,B错误;
C.由于Ksp(AgI)<Ksp(AgBr)<Ksp(AgCl),三种溶液等体积等浓度混合后用AgNO3溶液滴定,沉淀顺序为I-、Br-、Cl-,C正确;
D.当滴定AgNO3溶液至30.00mL时,c(I-)=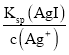 ,c(Br-)=
,c(Br-)=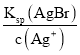 ,c(Cl-)=
,c(Cl-)=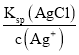 ,由于Ksp(AgI)<Ksp(AgBr)<Ksp(AgCl),则平衡时c(I-)<c(Br-)<c(Cl-),D正确;
,由于Ksp(AgI)<Ksp(AgBr)<Ksp(AgCl),则平衡时c(I-)<c(Br-)<c(Cl-),D正确;
故合理选项是B。

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目