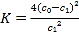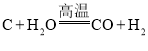题目内容
【题目】锂电池是新型高能电池,它以质量轻、能量高而受到了普遍重视,目前已研制成功多种锂电池。某种锂电池的总反应为:Li+MnO2=LiMnO2,下列说法正确的是( )
A.锂是正极,电极反应为:Li-e-=Li+B.锂是负极,电极反应为:Li-e-=Li+
C.锂是负极,电极反应为:MnO2+e-=MnO![]() D.锂是负极,电极反应为:Li-2e-=Li2+
D.锂是负极,电极反应为:Li-2e-=Li2+
【答案】B
【解析】
A.根据锂电池的总反应式Li+MnO2=LiMnO2,失电子的金属Li为负极,电极反应为:Li-e-=Li+,选项A错误;
B.根据锂电池的总反应式Li+MnO2=LiMnO2,失电子的金属Li为负极,电极反应为:Li-e-=Li+,选项B正确;
C.MnO2是正极,电极反应为MnO2+e-=MnO2-,选项C错误;
D.根据锂电池的总反应式Li+MnO2=LiMnO2,失电子的金属Li为负极,电极反应为:Li-e-=Li+,选项D错误。
答案选B。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】著名化学家徐光宪在稀土领域贡献突出,被誉为“稀土界的袁隆平”。钇是稀土元素之一,我国蕴藏着丰富的钇矿石![]() ,工业上通过如下工艺流程制取氧化钇,并获得副产物铍。
,工业上通过如下工艺流程制取氧化钇,并获得副产物铍。
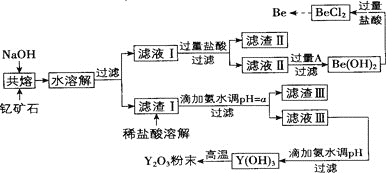
已知:
![]() 钇
钇![]() 的常见化合价为
的常见化合价为![]() 价;
价;
![]() 铍和铝处于元素周期表的对角线位置,化学性质相似;
铍和铝处于元素周期表的对角线位置,化学性质相似;
![]() 、
、![]() 形成氢氧化物沉淀时的pH如下表:
形成氢氧化物沉淀时的pH如下表:
离子 | 开始沉淀时的pH | 完全沉淀时的pH |
Fe3+ | 2:1 | 3:1 |
Y3+ | 6.0 | 8.3 |
![]() 将钇矿石与NaOH共熔的反应方程式补充完整:
将钇矿石与NaOH共熔的反应方程式补充完整:
_____![]() _____
_____![]() _____
_____![]() _____
_____![]() _____
_____![]() _____
_____![]() _____
_____![]() _____
_____![]()
![]() 滤渣Ⅱ的主要成分是_________。
滤渣Ⅱ的主要成分是_________。
![]() 试剂A可以是_________
试剂A可以是_________![]() 填序号
填序号![]() 。
。
A NaOH溶液 ![]() 氨水
氨水 ![]()
![]()
![]() 用氨水调节
用氨水调节![]() 时,a的取值范围是_____________。
时,a的取值范围是_____________。
![]() 计算常温下
计算常温下![]() 的平衡常数
的平衡常数![]() ____________。
____________。![]() 常温下
常温下![]()
![]() 滤液Ⅲ加入氨水产生沉淀的离子方程式为___________。
滤液Ⅲ加入氨水产生沉淀的离子方程式为___________。
![]() 从
从![]() 溶液中得到
溶液中得到![]() 固体的操作是_______。
固体的操作是_______。