题目内容
【题目】化工生产中常用FeS作为沉淀剂除去工业废水中的Pb2+,反应原理为FeS(s)+Pb2+(aq) ![]() PbS(s)+Fe2+(aq),下列有关叙述错误的是( )
PbS(s)+Fe2+(aq),下列有关叙述错误的是( )
A.达到平衡时,c(Pb2+)=c(Fe2+)
B.Ksp(FeS)大于Ksp(PbS)
C.该反应的平衡常数K=
D.溶液中加入少量Na2S固体后,c(Fe2+)减小
【答案】A
【解析】
A. 该反应达到平衡时各离子的浓度保持不变,但不一定相等,A错误;
B. 对于化合物构型相同的物质,溶度积大的沉淀容易转化为溶度积小的沉淀,所以FeS的Ksp(FeS)大于PbS的Ksp(PbS),B正确;
C. 反应的平衡常数 ,C正确;
,C正确;
D. 反应达到平衡后,向溶液中加入少量Na2S固体,c(S2-)增大,Fe2+、Pb2+会与S2-结合形成FeS、PbS沉淀,最终溶液中Fe2+、Pb2+均减小,D正确;
故合理选项是A。

 科学实验活动册系列答案
科学实验活动册系列答案【题目】天青石(主要含有SrSO4和少量CaCO3杂质)是获取锶元素的各种化合物的主要原料。回答下列问题(相关数据如下):
温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
Sr(OH)2 | 0.91 | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
ⅡA元素氢氧化物 | Be(OH)2 | Mg(OH)2 | Ca(OH)2 | Sr(OH)2 | Ba(OH)2 | ||||
25℃时饱和溶液浓度molL-1 | 8.00×10-6 | 5.00×10-4 | 2.00×10-2 | 6.00×10-2 | 2.00×10-1 | ||||
I.(1)SrO2中氧元素的化合价为___。Sr(OH)2的碱性比Mg(
(2)工业上可以用SrO与铝粉充分混合,在真空加热反应生成金属锶和3SrO8Al2O3,写出该反应的化学方程式___。
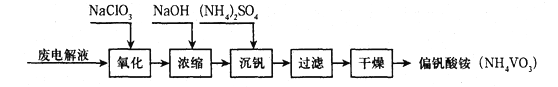
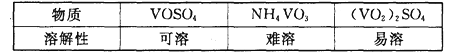
Ⅱ.以天青石(主要含有SrSO4和少量CaCO3杂质)生产Sr(OH)2xH2O的工艺如下:

(3)滤渣2为混有CaCO3的SrCO3,写出生成SrCO3的化学方程式___。
(4)加热水浸固体3是为了获得较为纯净的Sr(OH)2涪液,此时应缓慢加热使沉淀颗粒长大,有利于___。
(5)从趁热过滤后的滤液中得到Sr(OH)2xH2O产品的步骤为降温结晶、过滤、洗涤、干燥。为得到较大颗粒的Sr(OH)2xH2O晶体,可采用的方法是___(填一种)。
(6)取m g纯净Sr(OH)2xH2O产品溶于水,加入过量纯碱溶液后过滤、洗涤、干燥后,得到n g滤渣,则x=___(用含m、n的式子表示)。