题目内容
【题目】天青石(主要含有SrSO4和少量CaCO3杂质)是获取锶元素的各种化合物的主要原料。回答下列问题(相关数据如下):
温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
Sr(OH)2 | 0.91 | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
ⅡA元素氢氧化物 | Be(OH)2 | Mg(OH)2 | Ca(OH)2 | Sr(OH)2 | Ba(OH)2 | ||||
25℃时饱和溶液浓度molL-1 | 8.00×10-6 | 5.00×10-4 | 2.00×10-2 | 6.00×10-2 | 2.00×10-1 | ||||
I.(1)SrO2中氧元素的化合价为___。Sr(OH)2的碱性比Mg(
(2)工业上可以用SrO与铝粉充分混合,在真空加热反应生成金属锶和3SrO8Al2O3,写出该反应的化学方程式___。
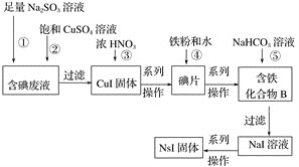
Ⅱ.以天青石(主要含有SrSO4和少量CaCO3杂质)生产Sr(OH)2xH2O的工艺如下:

(3)滤渣2为混有CaCO3的SrCO3,写出生成SrCO3的化学方程式___。
(4)加热水浸固体3是为了获得较为纯净的Sr(OH)2涪液,此时应缓慢加热使沉淀颗粒长大,有利于___。
(5)从趁热过滤后的滤液中得到Sr(OH)2xH2O产品的步骤为降温结晶、过滤、洗涤、干燥。为得到较大颗粒的Sr(OH)2xH2O晶体,可采用的方法是___(填一种)。
(6)取m g纯净Sr(OH)2xH2O产品溶于水,加入过量纯碱溶液后过滤、洗涤、干燥后,得到n g滤渣,则x=___(用含m、n的式子表示)。
【答案】-1 强 5.00×10-10 27SrO+16Al![]() 3SrO8Al2O3+24Sr SrSO4+2NH4HCO3=SrCO3↓+H2O+CO2↑+(NH4)2SO4 过滤分离 减慢冷却结晶的速度
3SrO8Al2O3+24Sr SrSO4+2NH4HCO3=SrCO3↓+H2O+CO2↑+(NH4)2SO4 过滤分离 减慢冷却结晶的速度 ![]()
【解析】
天青石(主要成分SrSO4)粉碎后与NH4HCO3混合加热,发生反应有(NH4)2SO4和CO2、SrCO3,然后过滤,在滤渣中含有SrCO3,将其煅烧,反应产生SrO,SrO与水反应产生Sr(OH)2x H2O。据此解答。
I.(1)Sr的化合价为+2,SrO2中氧元素的化合价为-1;25℃时,饱和Sr(OH)2溶液的浓度大于Mg(OH)2的浓度,即Sr(OH)2溶液电离程度大、碱性强;25℃时Mg(OH)2的溶度积Ksp=c(Mg2+)×c2(OH-)=5.00×10-4×(2×5.00×10-4)2=5.00×10-10;
(2)SrO与铝粉加热反应生成金属锶和3SrO8Al2O3,反应的化学方程式为27SrO+16Al![]() 3SrO8Al2O3+24Sr;
3SrO8Al2O3+24Sr;
II.(3)滤渣2混有SrCO3,则SrSO4和NH4HCO3反应生成SrCO3的化学方程式为SrSO4+2NH4HCO3=SrCO3↓+H2O+CO2↑+(NH4)2SO4;
(4)加热水浸固体3是为了获得较为纯净的Sr(OH)2溶液,缓慢加热有利于沉淀颗粒长大,便于过滤分离;
(5)从趁热过滤后的滤液中得到Sr(OH)2xH2O产品的步骤为降温结晶、过滤等。所以要得到较大颗粒的Sr(OH)2xH2O晶体,可减慢冷却结晶的速度;
(6)将m g纯净Sr(OH)2·xH2O产品溶于水,加入过量纯碱溶液,发生反应产生SrCO3、NaOH,由Sr原子守恒得到关系式:Sr(OH)2xH2O~SrCO3,根据二者反应关系式可知:每(122+18x)份Sr(OH)2xH2O反应会产生88份SrCO3,则m g Sr(OH)2xH2O反应产生SrCO3的质量为m(SrCO3)=![]() ×m g=n g,解得x=
×m g=n g,解得x=![]() 。
。

【题目】锶(Sr)元素广泛存在于矿泉水中,是一种人体必需的微量元素,在元素周期表中与钙和钡属于第ⅡA族元素。
(1)碱性:Sr(OH)2___Ba(OH)2(填“<”或“>”;锶的化学性质与钙和钡类似,用原子结构的观点解释其原因是___。
(2)碳酸锶是最重要的锶化合物。用含SrSO4和少量BaSO4、BaCO3、FeO、Fe2O3、Al2O3、SiO2的天青石制备SrCO3,工艺流程如下(部分操作和条件略):
Ⅰ.将天青石矿粉和碳酸钠溶液混合后充分反应,过滤;
Ⅱ.向滤渣中加入足量盐酸充分反应,过滤;
Ⅲ.向Ⅱ所得滤液中加入足量的稀硫酸,过滤;
Ⅳ.向Ⅲ所得滤液中先加入氯水,充分反应后再用氨水调pH约为7,过滤;
Ⅴ.向Ⅳ所得滤液中加入稍过量的碳酸氢铵溶液,充分反应后过滤,将沉淀洗净,烘干,得SrSO3。
已知:ⅰ.相同温度时溶解度:BaSO4<SrCO3<SrSO4<CaSO4
ⅱ.生成氢氧化物沉淀的pH如下表所示:
物质 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
开始沉淀的pH | 1.9 | 7.0 | 3.4 |
完全沉淀的pH | 3.2 | 9.0 | 4.7 |
①步骤Ⅰ中,反应的化学方程式是______。为提高此步骤中锶的转化效果可以采取的措施有(任答两点即可):______。
②步骤Ⅱ中,能与盐酸反应而溶解的物质有______。
③步骤Ⅳ的目的是_______。
④下列关于该工艺流程的说法正确的是________(填字母代号)。
a.该工艺产生的废液含较多的NH4+、Na+、SO42-、Cl-
b.SiO2在步骤Ⅰ操作时被过滤除去
c.步骤Ⅴ中反应时,加入NaOH溶液可以提高NH4HCO3的利用率