题目内容
【题目】高炉炼铁过程中发生的反应:1/3Fe2O3(s)+CO(g)2/3Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下表,下列说法正确的是
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
A. △H>0
B. 该反应的平衡常数表达式是![]()
C. 其他条件不变,向平衡体系充入CO2气体,K值减小
D. 其他条件不变,增大压强,平衡往逆向移动
【答案】B
【解析】
A、依据图表数据分析,平衡常数随温度升高减小,平衡逆向进行,逆向是吸热反应,正反应是放热反应,△H<0,故A错误;
B、依据化学方程式和平衡常数概念书写平衡常数表达式,注意固体和纯液体不能写入表达式,平衡常数K=![]() ,故B正确;
,故B正确;
C、平衡常数随温度变化,不随浓度变化,其他条件不变,向平衡体系充入CO2气体,K值不变,故C错误;
D、由反应式:1/3Fe2O3(s)+CO(g)2/3Fe(s)+CO2(g)可知,反应前后气体体积不变,故其他条件不变,增大压强,平衡不移动,故D错误。
故选B。

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案【题目】I、在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量![]() N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256kJ的热量.
N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256kJ的热量.
(1)写出该反应的热化学方程式_______________________________________.
(2)已知H2O(l)═H2O(g);△H=+44kJ·mol﹣1,则16g液态肼燃烧生成氮气和液态水时,放出的热量是________kJ.
(3)丙烷燃烧可以通过以下两种途径:
途径I:C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=﹣a kJ·mol﹣1
途径II:C3H8(g)═C3H6(g)+H2(g)△H=+b kJ·mol﹣1
2C3H6(g)+9O2(g)═6CO2(g)+6H2O(l)△H=﹣c kJ·mol﹣1
2H2(g)+O2 (g)═2H2O(l)△H=﹣d kJ·mol﹣1 (abcd均为正值)
请回答下列问题:
①判断等量的丙烷通过两种途径放出的热量,途径I放出的热量_______(填“大于”、“等于”或“小于”)途径II放出的热量.
②在C3H8(g)═C3H6(g)+H2(g) 的反应中,反应物具有的总能量________(填“大于”、“等于”或“小于”)生成物具有的总能量.
③b 与a、c、d的数学关系式是_____________.
II、利用如图所示装置测定中和热的实验步骤如下:
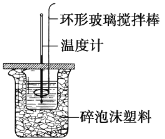
①用量筒量取50 mL 0.50 mol·L1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50 mL 0.55 mol·L1 NaOH溶液,并用同一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
(1)为什么所用NaOH溶液要稍过量?__________________________。
(2)假设盐酸和氢氧化钠溶液的密度都是1 g·cm3,又知中和反应后生成溶液的比热容c=4.18 J·g1·℃1。为了计算中和热,某学生实验记录数据如下:
实验 序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | 氢氧化钠 | ||
1 | 20.0 | 20.0 | 23.0 |
2 | 20.1 | 20.1 | 23.2 |
3 | 20.2 | 20.2 | 23.4 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=________kJ·mol1_(结果保留一位小数)。
(3)不能用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸,理由是_________________。
【题目】GaN是制造5G芯片的材料,氮化镓铝和氮化铝LED可发出紫外光。回答下列问题:
(1)基态As原子核外电子排布式为[Ar]___,下列状态的铝中,电离最外层的一个电子所需能量最小的是___(填标号)。
A.![]() B.
B.![]() C.[Ne] D.
C.[Ne] D.![]()
(2)8一羟基喹啉铝(分子式C27H18AlN3O3)用于发光材料及电子传输材料,可由LiAlH4与(8一羟基喹啉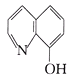 )合成。LiAlH4中阴离子的空间构型为____;所含元素中电负性最大的是___(填元素符号),C、N、O的杂化方式依次为____、_____和____。
)合成。LiAlH4中阴离子的空间构型为____;所含元素中电负性最大的是___(填元素符号),C、N、O的杂化方式依次为____、_____和____。
(3)已知下列化合物的熔点:
化合物 | AlF3 | GaF3 | AlCl3 |
熔点/°C | 1040 | 1000 | 194 |
①表中卤化物的熔点产生差异的原因是_____。
②熔融AlCl3时可生成具有挥发性的二聚体Al2Cl6,二聚体Al2Cl6的结构式为____;其中Al的配位数为____。
(4)GaAs的晶胞结构如图所示,其晶胞参数为apm。
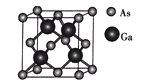
①紧邻的As原子之间的距离为x,紧邻的As、Ga原子之间的距离为y,则![]() __。
__。
②设阿伏加德罗常数的值为NA,则GaAs的密度是___g·cm一3(列出计算表达式)。




