题目内容
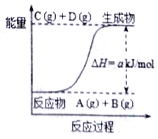
【题目】已知分解1mol KClO3放出热量38.8kJ,在存在MnO2条件下加热,KClO3的分解机理为:
①2KClO3+4MnO2=2KCl+2Mn2O7 慢 ②2Mn2O7=4MnO2+3O2 快
下列有关说法中不正确的是( )
A. 1mol KClO3所具有的总能量高于1mol KCl和1.5mol O2所具有的总能量
B. KClO3分解速率快慢主要取决于反应①
C. 1g KClO3、1g MnO2和0.1g Mn2O7混合加热,充分反应后MnO2质量为1g
D. 将固体二氧化锰碾碎,可加快KClO3的分解速率
【答案】C
【解析】
A.分解1molKClO3放出热量38.8kJ,可知分解反应为放热反应;
B.慢反应为决定反应速率的主要因素;
C.由反应②可知,Mn2O7分解会生成一部分MnO2;
D.催化剂的接触面积增大,可加快反应速率。
A.反应2KClO3![]() 2KCl+3O2↑为放热反应,说明1molKClO3所具有的总能量高于1molKCl和1.5molO2所具有的总能量之和,A正确;
2KCl+3O2↑为放热反应,说明1molKClO3所具有的总能量高于1molKCl和1.5molO2所具有的总能量之和,A正确;
B.由分解机理可知,KClO3的分解速率取决于慢反应,即取决于反应①,B正确;
C.由反应②可知,0.1gMn2O7分解会生成一部分MnO2,故反应后MnO2的总质量大于1g,C错误;
D.由分解机理可知,KClO3的分解速率取决于慢反应,即由反应①决定,将固体二氧化锰碾碎,由于固体表面积增大,所以可加快反应①的反应速率,D正确;
故合理选项是C。

【题目】某无色稀溶液X中,可能含有下表所列离子中的某几种。
阴离子 | CO32-、SiO32-、AlO2-、Cl- |
阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示。
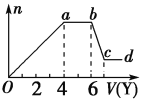
(1)若Y是盐酸,则oa段转化为沉淀的离子(指来源于X溶液的,下同)是________________________,ab段发生反应的离子是________,bc段发生反应的离子方程式为___________________________________。
(2)若Y是NaOH溶液,则X中一定含有的阳离子是____________________, ab段反应的离子方程式为_______________________________________________________________________。
【题目】高炉炼铁过程中发生的反应:1/3Fe2O3(s)+CO(g)2/3Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下表,下列说法正确的是
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
A. △H>0
B. 该反应的平衡常数表达式是![]()
C. 其他条件不变,向平衡体系充入CO2气体,K值减小
D. 其他条件不变,增大压强,平衡往逆向移动