题目内容
【题目】下列关于电子式的表述正确的是( )
A.HClO的电子式为
B.SCl2的电子式为
C.用电子式表示HCl的形成过程为
![]()
D.已知SCN-每个原子都达到8电子结构,则其电子式为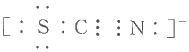
【答案】D
【解析】
A.HClO是共价化合物,氯原子最外层有7个电子,氧原子最外层有6个电子,各原子要达到稳定结构,氯需形成1对共价键,氧需形成2对共价键,故HClO电子式应为![]() ,故A错误;
,故A错误;
B.硫原子最外层有6个电子,氯原子最外层有7个电子,硫原子应分别与2个氯原子形成1对共用电子对,从而达到8电子稳定结构,故其正确的电子式应为![]() ,故B错误;
,故B错误;
C.HCl为共价化合物,以共用电子对成键,用电子式表示HCl的形成过程为![]() ,故C错误;
,故C错误;
D.SCN中S、C.N原子都达到8电子结构,其电子式为 ,故D正确;
,故D正确;
答案选D。

练习册系列答案
相关题目
【题目】某化学兴趣小组同学用 NaHCO3和KHCO3组成的某均匀混合物进行实验,测得如下数据(盐酸的物质的量浓度相等)
实验序号 | I | II | III |
盐酸体积(mL) | 100.0 | 100.0 | 100.0 |
样品质量/g | 9.2 | 15.7 | 27.6 |
CO2体积/L (标准状况) | 2.24 | 3.36 | 3.36 |
(1)该盐酸的物质的量浓度为______mol·Lˉ1
(2)使盐酸恰好完全反应,所需要的样品质量为______g