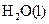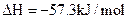题目内容
对比以下几个反应式:
Cl+Cl=Cl2△H=-247kJ?mol-1
O+O=O2△H=-493kJ?mol-1
N+N=N2△H=-946kJ?mol-1
可以得出的结论是( )
Cl+Cl=Cl2△H=-247kJ?mol-1
O+O=O2△H=-493kJ?mol-1
N+N=N2△H=-946kJ?mol-1
可以得出的结论是( )
| A.在常温下氮气比氧气、氯气都稳定 |
| B.氮、氧、氯的单质常温下为气体 |
| C.氮、氧、氯的单质氧化性依次增强 |
| D.氮气、氧气和氯气的密度不同 |
反应式给出的原子结合成分子放出的热量,为原子间的键能,物质的键能越大,断裂时需要吸收的热量越多,越稳定,不能用于判断气体的沸点、密度以及氧化性强弱,
故选A.
故选A.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
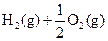 ══
══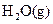
 ══
══
 ══
══
 ══
══