题目内容
3.在下列叙述中,不正确的是( )| A. | 40K和40Ca原子中的质子数和中子数都不相等 | |
| B. | H2和D2互为同位素 | |
| C. | 互为同位素的原子,它们的原子核内的中子数一定不相等 | |
| D. | 互为同位素的原子,它们原子核内的质子数一定相等 |
分析 A.质子数+中子数=质量数;
B.H2和D2为单质,而同位素的分析对象为原子;
C.D.具有相同质子数,不同中子数或同一元素的不同核素互为同位素.
解答 解:A.40K的质子数为19,中子数为40-19=21,40Ca的质子数与中子数都是20,二者的质子数和质子数不相等,故A正确;
B.H2和D2为单质,二者为同种物质,而同位素的分析对象为原子,故B错误;
C.互称为同位素的两种核素之间具有相同数值的是质子数,中子数不同,故C正确;
D.互称为同位素的两种核素之间具有相同数值的是质子数,故D正确.
故选B.
点评 本题考查原子的构成、同位素等知识,题目难度不大,试题注重基础知识的考查,注意了解同位素的概念及判断方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.下表列出了①~⑥六种元素在元素周期表中的位置.
请回答下列问题:
(1)③的元素符号是Mg.
(2)②、③、④三种元素相比较,金属性最强的是Na (填写元素符号);
(3)元素⑤和⑥的氢化物中,稳定性较强的是HF(填氢化物的分子式);
(4)④的最高价氧化物对应的水化物的化学式为Al(OH)3;
(5)画出元素③的原子结构示意图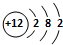 ;
;
(6)元素③的单质与盐酸反应的离子方程式为Mg+2H+=Mg2++H2↑;
(7)元素②形成的盐如:碳酸钠.当碳酸钠中含有碳酸氢钠杂质时,除去此杂质的简单方法是加热(填“萃取”或“加热”或“蒸馏”).
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ⑤ | ||||||
| 3 | ② | ③ | ④ | ⑥ |
(1)③的元素符号是Mg.
(2)②、③、④三种元素相比较,金属性最强的是Na (填写元素符号);
(3)元素⑤和⑥的氢化物中,稳定性较强的是HF(填氢化物的分子式);
(4)④的最高价氧化物对应的水化物的化学式为Al(OH)3;
(5)画出元素③的原子结构示意图
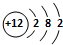 ;
;(6)元素③的单质与盐酸反应的离子方程式为Mg+2H+=Mg2++H2↑;
(7)元素②形成的盐如:碳酸钠.当碳酸钠中含有碳酸氢钠杂质时,除去此杂质的简单方法是加热(填“萃取”或“加热”或“蒸馏”).
11.对于N2(g)+3H2(g)?2NH3(g)△H<0的反应,达到化学平衡状态的标志为( )
| A. | 断开1个N≡N键的同时有6个N-H键生成 | |
| B. | 混合气体的密度不变 | |
| C. | 混合气体的平均相对分子质量不变 | |
| D. | N2、H2、NH3分子数之比为1:3:2的状态 |
18.对于锌粒和稀H2SO4的反应,下列说法中不正确的是( )
| A. | 可选用颗粒大小基本相同的锌粒与等体积不同浓度的硫酸反应,比较二者收集10mL H2所用的时间,从而计算反应速率并说明浓度对反应速率的影响 | |
| B. | 可选用等质量的锌片和锌粒与相同浓度的硫酸反应,记录锌完全消失的时间,从而计算反应速率并说明固体表面积对反应速率的影响 | |
| C. | 可记录溶液中c(H+) 随时间的变化(用pH计测定溶液的pH)来测量反应速率 | |
| D. | 可记录溶液的温度变化(用温度计测量温度)来测量反应速率 |
15.已知-CN是直线型结构,下列有机分子中,所有的原子不可能处在同一个平面内的是( )
| A. | CH2=CH-CN | B. | CH2=CH-CH=CH2 | C. | CH2=C(CH3)-CH=CH2 | D. | CH3CH3 |
17.在下列物质间相互变化中,需要加入氧化剂才能实现的是( )
| A. | H2SO4→MgSO4 | B. | NaCl→Cl2 | C. | CuSO4→Cu | D. | HClO→Cl2 |