题目内容
13.下表列出了①~⑥六种元素在元素周期表中的位置.| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ⑤ | ||||||
| 3 | ② | ③ | ④ | ⑥ |
(1)③的元素符号是Mg.
(2)②、③、④三种元素相比较,金属性最强的是Na (填写元素符号);
(3)元素⑤和⑥的氢化物中,稳定性较强的是HF(填氢化物的分子式);
(4)④的最高价氧化物对应的水化物的化学式为Al(OH)3;
(5)画出元素③的原子结构示意图
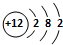 ;
;(6)元素③的单质与盐酸反应的离子方程式为Mg+2H+=Mg2++H2↑;
(7)元素②形成的盐如:碳酸钠.当碳酸钠中含有碳酸氢钠杂质时,除去此杂质的简单方法是加热(填“萃取”或“加热”或“蒸馏”).
分析 (1)由元素在周期表中的位置可知,①为Li、②为Na、③为Mg、④为Al、⑤为F、⑥为Cl;
(2)同周期自左而右元素金属性减弱;
(3)元素非金属性越强,对应氢化物越稳定;
(4)④的最高价氧化物对应的水化物为氢氧化铝;
(5)③为Mg,原子核外有12个电子,有3个电子层,各层电子数为2、8、2;
(6)镁与盐酸反应生成氯化镁与氢气;
(7)碳酸氢钠加热分解得到碳酸钠,用加热方法除去碳酸钠中含有碳酸氢钠杂质.
解答 解:(1)由元素在周期表中的位置可知,①为Li、②为Na、③为Mg、④为Al、⑤为F、⑥为Cl,故答案为:Mg;
(2)同周期自左而右元素金属性减弱,故金属性:Na>Mg>Al,故答案为:Na;
(3)同主族自上而下元素非金属性减弱,元素非金属性越强,对应氢化物越稳定,故氢化物稳定性:HF>HCl,故答案为:HF;
(4)④的最高价氧化物对应的水化物为Al(OH)3,故答案为:Al(OH)3;
(5)③为Mg,原子核外有12个电子,有3个电子层,各层电子数为2、8、2,原子结构示意图为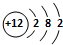 ,故答案为:
,故答案为: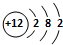 ;
;
(6)镁与盐酸反应生成氯化镁与氢气,反应离子方程式为:Mg+2H+=Mg2++H2↑,故答案为:Mg+2H+=Mg2++H2↑;
(7)碳酸氢钠加热分解得到碳酸钠,用加热方法除去碳酸钠中含有碳酸氢钠杂质,故答案为:加热.
点评 本题考查元素周期表与元素周期律的应用,比较基础,需要学生熟练掌握短周期元素,侧重对基础知识的巩固.

练习册系列答案
 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
1.某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol•L-1盐酸、0.55mol•L-1NaOH溶液,实验尚缺少的玻璃用品是量筒、温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?不能(填“能”或“否”),其原因是金属易导热,热量散失导致误差大.
(3)他们记录的实验数据如下:
已知:Q=cm(t2-t1),反应后溶液的比热容c为4.18J•℃-1•g-1,各物质的密度均为1g•cm-3.
①计算完成上表△H=-56.85(保留2位小数).
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l)△H=-56.8kJ•mol-1.
(4)若用KOH代替NaOH,对测定结果无(填“有”或“无”)影响;若用醋酸代替HCl做实验,对测定结果有填“有”或“无”)影响.
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol•L-1盐酸、0.55mol•L-1NaOH溶液,实验尚缺少的玻璃用品是量筒、温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?不能(填“能”或“否”),其原因是金属易导热,热量散失导致误差大.
(3)他们记录的实验数据如下:
| 实验用品 | 溶液温度 | 中和热 | ||
| t1 | t2 | △H | ||
| ① | 50 mL0.55 mol•L-1NaOH溶液 | 20℃ | 23.3℃ | |
| 50 mL0.5 mol•L-1HCl溶液 | ||||
| ② | 50 mL0.55 mol•L-1NaOH溶液 | 20℃ | 23.5℃ | |
| 50 mL0.5 mol•L-1HCl溶液 | ||||
①计算完成上表△H=-56.85(保留2位小数).
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l)△H=-56.8kJ•mol-1.
(4)若用KOH代替NaOH,对测定结果无(填“有”或“无”)影响;若用醋酸代替HCl做实验,对测定结果有填“有”或“无”)影响.
5.下列离子方程式书写正确的是( )
| A. | 氯水和碘化钾反应:Cl2+I-═Cl-+I2 | |
| B. | 碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | 氯气和水反应:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH- |
3.在下列叙述中,不正确的是( )
| A. | 40K和40Ca原子中的质子数和中子数都不相等 | |
| B. | H2和D2互为同位素 | |
| C. | 互为同位素的原子,它们的原子核内的中子数一定不相等 | |
| D. | 互为同位素的原子,它们原子核内的质子数一定相等 |
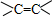 、醛基-CHO、羧基-COOH、-COOR酯基.
、醛基-CHO、羧基-COOH、-COOR酯基.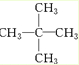 ,名称为2,2-二甲基丙烷.
,名称为2,2-二甲基丙烷.