题目内容
1.关于合成氨反应N2(g)+3H2(g)?2NH3(g)达到限度时,下列叙述正确的是( )| A. | N2和H2全部转化为NH3 | |
| B. | 正反应和逆反应的化学反应速率均为零 | |
| C. | N2、H2和NH3的物质的量浓度之比为1:3:2 | |
| D. | 若外界条件发生改变,化学反应的限度可能随之改变 |
分析 该反应为可逆反应,反应物不可能完全转化,当达到平衡状态时,正逆反应速率相等但不等于零,各物质的浓度不再发生改变,外界条件发生改变,可使平衡发生移动,据此分析.
解答 解:A. 合成氨的反应是可逆反应,反应物不可能完全转化,故A错误;
B.达到化学平衡时,正逆反应速率相等但不等于零,故B错误;
C.达到平衡状态是N2、H2和NH3的物质的量浓度之比不一定为1:3:2,与起始的量有关,故C错误;
D.外界条件发生改变,平衡发生移动,所以化学反应的限度可能随之改变,故D正确.
故选D.
点评 本题考查了化学平衡状态的定义,难度不大,注意化学平衡状态时,正逆反应速率相等但不等于0,且必须是同一物质的正逆反应速率相等.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
11.常温下,将等体积,等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7.下列关于滤液中的离子浓度关系不正确的是( )
| A. | c(H+)+c(NH4+ )=c(OH- )+c(HCO3-)+2c(CO32-) | |
| B. | c(Na+ )=c(HCO3-)+c(CO32-)+c(H2CO3) | |
| C. | $\frac{{K}_{w}}{c({H}^{+})}$<1.0×10-7mol/L | |
| D. | c(Cl-)>c(NH4+)>c(HCO3-)>c(CO32-) |
13.1mol•L-1 MgCl2溶液的含义是( )
| A. | 1 L水中含有1 mol MgCl2 | |
| B. | Cl-浓度为2 mol•L-1 | |
| C. | 溶液中含有1 mol MgCl2 | |
| D. | 将95 g MgCl2溶于1 L水中所得的溶液 |
11.下列关于SO2的叙述中,正确的是( )
| A. | SO2的摩尔质量是64g | |
| B. | 1molSO2中含氧原子数约为6.02×1023 | |
| C. | 常温常压下,1molSO2的体积为22.4L | |
| D. | 常温常压下,64gSO2的物质的量为1mol |
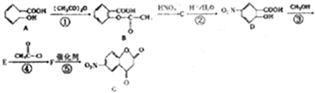
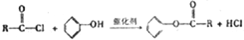
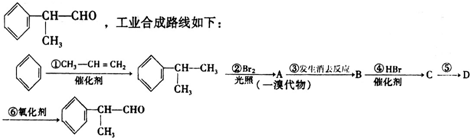
 .写出F与过量NaOH共热时反应的化学方程式
.写出F与过量NaOH共热时反应的化学方程式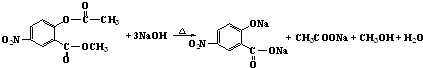 .
. 或
或 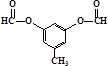 .
.
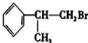 或
或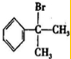 .
.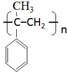 .
.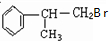 +NaOH$→_{△}^{H_{2}O}$NaBr+
+NaOH$→_{△}^{H_{2}O}$NaBr+ ,其反应类型为取代反应.
,其反应类型为取代反应. (或
(或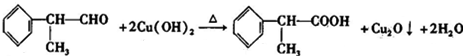 ).
).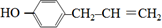 、
、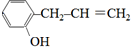 、
、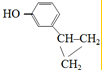 .
.